题目内容
1. 某小组用图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.
某小组用图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.(1)①中铜与浓硫酸反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)②中品红溶液的现象是红色褪去.
(3)③中NaOH溶液的作用是吸收多余的二氧化硫.
(4)①中铜丝可以上下抽动,其目的是可通过抽拉铜丝调节其与浓硫酸反应的发生与停止.
分析 (1)加热条件下,Cu和H2SO4(浓)反应生成CuSO4、SO2和H2O;
(2)二氧化硫能和有色物质反应生成无色物质而具有漂白性;
(3)二氧化硫属于酸性氧化物且有毒,能被碱性物质吸收;
(4)①中铜丝可以上下抽动,将铜丝与浓硫酸分离或接触而停止或发生反应.
解答 解:(1)加热条件下,Cu和H2SO4(浓)反应生成CuSO4、SO2和H2O,反应方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O;
(2)二氧化硫能和有色物质反应生成无色物质而具有漂白性,二氧化硫能漂白品红溶液而使品红溶液褪色,所以看到的现象是溶液红色褪去,
故答案为:红色褪去;
(3)二氧化硫属于酸性氧化物且有毒,不能直接排空,能和NaOH反应生成无毒的亚硫酸钠,所以能被碱性物质吸收,则氢氧化钠溶液目的是吸收多余的二氧化硫,
故答案为:吸收多余的二氧化硫;
(4)①中铜丝可以上下抽动,将铜丝与浓硫酸分离或接触而停止或发生反应,所以目的是可通过抽拉铜丝调节其与浓硫酸反应的发生与停止,
故答案为:可通过抽拉铜丝调节其与浓硫酸反应的发生与停止.
点评 本题以浓硫酸和铜反应为载体考查浓硫酸性质,明确实验原理是解本题关键,知道每个装置的作用,注意二氧化硫不能漂白酸碱指示剂.

练习册系列答案
相关题目
12.在一定条件下,某密闭容器中进行反应:
4NH3(g)+5O2(g)?4NO(g)+6H2O(g).反应开始时NH3的浓度是1.0mol/L,经过20s后,它的浓度变成了0.2mol/L,容器体积不变,在这20s内H2O的化学反应速率为( )
4NH3(g)+5O2(g)?4NO(g)+6H2O(g).反应开始时NH3的浓度是1.0mol/L,经过20s后,它的浓度变成了0.2mol/L,容器体积不变,在这20s内H2O的化学反应速率为( )
| A. | 0.04 mol/(L•s) | B. | 0.06 mol/(L•s) | C. | 0.6 mol/(L•s) | D. | 0.8 mol/(L•s) |
9.丙烯醛的结构简式为CH2=CH-CHO,下列叙述正确的是( )
| A. | 能使溴水褪色,不能使酸性KMnO4溶液褪色 | |
| B. | 在一定条件下,与等物质的量的氢气反应生成1-丙醇 | |
| C. | 能发生银镜反应,表现出氧化性 | |
| D. | 在一定条件下,能被氧化为丙烯酸 |
16.有关化学用语正确的是( )
| A. | 过氧化钠的电子式: | B. | 乙醇的分子式C2H5OH | ||
| C. | 硫离子的结构示意图: | D. | 乙酸的结构简式:C2H4O2 |
13.一定质量的下列各组物质的混合物,不管两者以何种质量比混合,充分燃烧后所生成的H2O的质量都相等,该混合物可能是( )
| A. | 乙醇和乙烯 | B. | 甲醛和葡萄糖 | C. | 乙烯和乙酸乙酯 | D. | 丙烷和乙醛 |
10.(1)A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如表所示:
根据上述信息,写出B的基态原子核外电子排布式1s22s22p63s2,预测A和氯元素形成的简单分子空间构型为直线型.
(2)钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,往其中一种配合物的溶液中加入AgNO3溶液时,无明显现象,往其溶液中加BaCl2溶液时若,产生白色沉淀,则该配合物的化学式为[Co(Br)(NH3)5]SO4,中心离子的配位数为6.
(3)参考下表中的物质熔点回答下列问题
根据上表数据解释钠的卤化物及碱金属的氯化物的熔点变化规律随阴阳离子的半径增大,熔降低点.
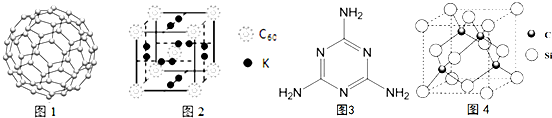
(4)C60可用作储氢材料.C60的结构如图1.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确不正确,并阐述理由C60是分子晶体,熔化时不需破坏化学键.科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体,该物质的K原子和C60分子的个数比为3:1.
 σ
σ
(5)三聚氰胺分子的结构简式如图3,则其中氮原子轨道杂化类型是sp2、sp3,l mol三聚氰胺分子中含15molσ键.
(6)碳化硅的晶胞与金刚石的晶胞相似如图4,设晶胞边长为a cm,碳原子直径为b cm,硅原子直径为c cm,则该晶胞的空间利用率为$\frac{2π({b}^{3}+{c}^{3})}{3{a}^{3}}$×100%.(用含a、b、c的式子表示).
| 电离能(KJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
(2)钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,往其中一种配合物的溶液中加入AgNO3溶液时,无明显现象,往其溶液中加BaCl2溶液时若,产生白色沉淀,则该配合物的化学式为[Co(Br)(NH3)5]SO4,中心离子的配位数为6.
(3)参考下表中的物质熔点回答下列问题
| 物质 | NaF | NaCl | NaBr | NaI | NaCl | KCl | RbCl | CsCl |
| 熔点(℃) | 995 | 801 | 755 | 651 | 801 | 776 | 715 | 646 |
(4)C60可用作储氢材料.C60的结构如图1.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确不正确,并阐述理由C60是分子晶体,熔化时不需破坏化学键.科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体,该物质的K原子和C60分子的个数比为3:1.
 σ
σ(5)三聚氰胺分子的结构简式如图3,则其中氮原子轨道杂化类型是sp2、sp3,l mol三聚氰胺分子中含15molσ键.
(6)碳化硅的晶胞与金刚石的晶胞相似如图4,设晶胞边长为a cm,碳原子直径为b cm,硅原子直径为c cm,则该晶胞的空间利用率为$\frac{2π({b}^{3}+{c}^{3})}{3{a}^{3}}$×100%.(用含a、b、c的式子表示).
11.下列各组物质中,都是共价化合物的是( )
| A. | H2O2和CaF2 | B. | H2S和Na2O2 | C. | HNO3和HClO4 | D. | NH3和N2 |




 乙烯雌酚是一种激素类药物,结构简式如图.
乙烯雌酚是一种激素类药物,结构简式如图. .
.