题目内容
16.对于可逆反应4NH3+5O2?4NO+6H2O(g),下列叙述正确的是( )| A. | 只有达到平衡时,消耗O2的速率与生成NO的速率之比才为5;4 | |
| B. | 若单位时间生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态 | |
| C. | 达到平衡状态后,NH3、O2、NO、H2O(g)的物质的量保持不变 | |
| D. | 达到平衡状态时,若增加容器体积,则反应速率增大 |
分析 A、反应进行的任何状态,消耗O2的速率与生成NO的速率之比都等于系数之比;
B、化学平衡的特征:正逆反应速率相等;
C、化学平衡的特征:组分的浓度(物质的量)不随时间的变化而变化;
D、达到平衡状态时,若增加容器体积,压强会减小,根据压强对化学反应速率的影响来回答.
解答 解:A、反应进行的任何状态,消耗O2的速率与生成NO的速率之比都等于系数之比,不一定是平衡状态,故A错误;
B、若单位时间生成xmolNO的同时,消耗xmolNH3,不能说明正逆反应速率相等,故B错误;
C、化学平衡的特征:组分的浓度(物质的量)不随时间的变化而变化,即NH3、O2、NO、H2O(g)的物质的量保持不变的状态一定是平衡状态,故C正确;
D、达到平衡状态时,若增加容器体积,压强会减小,化学反应速率会减慢,故D错误.
故选C.
点评 化学平衡状态的判断、化学平衡移动的方向以及影响化学平衡移动的因素是现在考查的热点,注意知识的归纳和整理,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列是元素周期表的一部分
根据以上元素在周期表中的位置,用化学式填写空白.
(1)单质中氧化性最强的是F2,其电子式是 ;化学性质最不活泼的是Ne,A与D形成的阳离子的电子式是
;化学性质最不活泼的是Ne,A与D形成的阳离子的电子式是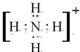 .
.
(2)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是NaOHAl(OH)3H3PO4HClO4;
(3)B元素可以形成两种氧化物,分别写出两种氧化物的电子式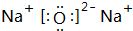 ,
,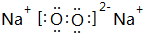 .其中B元素的原子与氧原子按1:1的个数比形成的化合物11.7g与足量二氧化碳完全反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2,有0.15mol 电子发生转移.
.其中B元素的原子与氧原子按1:1的个数比形成的化合物11.7g与足量二氧化碳完全反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2,有0.15mol 电子发生转移.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | A | |||||||
| 二 | D | F | H | |||||
| 三 | B | C | E | G |
(1)单质中氧化性最强的是F2,其电子式是
 ;化学性质最不活泼的是Ne,A与D形成的阳离子的电子式是
;化学性质最不活泼的是Ne,A与D形成的阳离子的电子式是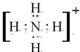 .
.(2)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是NaOHAl(OH)3H3PO4HClO4;
(3)B元素可以形成两种氧化物,分别写出两种氧化物的电子式
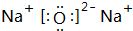 ,
, .其中B元素的原子与氧原子按1:1的个数比形成的化合物11.7g与足量二氧化碳完全反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2,有0.15mol 电子发生转移.
.其中B元素的原子与氧原子按1:1的个数比形成的化合物11.7g与足量二氧化碳完全反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2,有0.15mol 电子发生转移.
11.下列各组物质中,都是共价化合物的是( )
| A. | H2O2和CaF2 | B. | H2S和Na2O2 | C. | HNO3和HClO4 | D. | NH3和N2 |
1.与氢气完全加成后,不可能生成2,2,3-三甲基戊烷的烃是( )
| A. | CH2=C(CH2CH3)C (CH3)3 | B. | CH2=C(CH3)C(CH3)2CH2CH3 | ||
| C. | HC≡CCH(CH3)C(CH3)3 | D. | (CH3)3CC(CH3)=CHCH3 |
19.下列化学式及结构式中,从成键情况看不合理的是( )
| A. | CH4Si: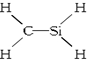 | B. | CH4S: | C. | CH2SeO: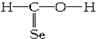 | D. | CH3N: |
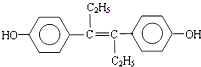 乙烯雌酚是一种激素类药物,结构简式如图.
乙烯雌酚是一种激素类药物,结构简式如图.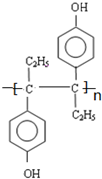 .
.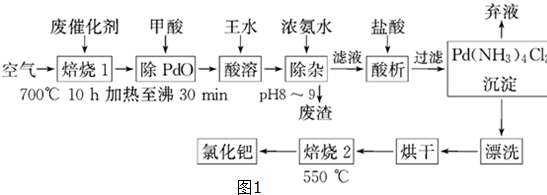
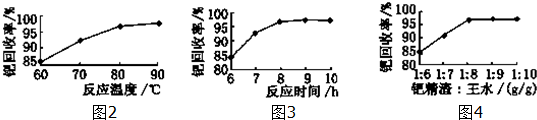
 某浅绿色晶体X[x(NH4)2SO4•yFeSO4•zH2O]在分析化学上常用作还原剂.为确定其组成,某小组同学进行如下实验.
某浅绿色晶体X[x(NH4)2SO4•yFeSO4•zH2O]在分析化学上常用作还原剂.为确定其组成,某小组同学进行如下实验.