��Ŀ����
14�����й����������ʱ仯�ıȽϣ�����ȷ���ǣ�������| A�� | ����ǿ����H2SiO3��H2CO3��HNO3 | B�� | ԭ�Ӱ뾶��С��Na��S��O | ||
| C�� | ����ǿ����KOH��NaOH��LiOH | D�� | �ǽ�����ǿ����I��Cl��F |
���� A��Ԫ�صķǽ�����Խǿ����Ӧ������������ˮ���������Խǿ��
B��ͬ����Ԫ�ش��ϵ��£�Ԫ�ذ뾶������ͬһ���ڣ�ԭ������Խ�뾶ԽС��
C��Ԫ�صĽ�����Խǿ����Ӧ�����������ļ���Խǿ��
D��ͬ��Ԫ�أ�ԭ������Խ�ǽ�����Խ����
��� �⣺A���ǽ�����N��C��Si��Ԫ�صķǽ�����Խǿ����Ӧ������������ˮ���������Խǿ����A��ȷ��
B��ͬ����Ԫ�ش��ϵ��£�Ԫ�ذ뾶������ͬһ���ڣ�ԭ��������С����Na��S��O����B��ȷ��
C��������K��Na��Li�������KOH��NaOH��LiOH����C��ȷ��
D��ͬ��Ԫ�أ�ԭ������Խ�ǽ�����Խ������F��Cl��I����D����ѡD��
���� ���⿼��Ԫ�������ɵĵݱ���ɣ�������ѧ���ķ��������ͻ���������ۺ���������õĿ��飬ע�����Ԫ�����Ӧ���ʡ�����������ʵ������Ժ͵ݱ��Ե��жϣ�ע�ػ���֪ʶ�Ļ��ۣ��ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
5�� ���ӽ����̸��Ŀ��2010��10�±������׳ơ�һ���㡱���ж����ʱ���ʳ�ú�����˸��࣬�����°�����һ���㡱�ķ��ӽṹ��ͼ��ʾ������˵����ȷ���ǣ�������
���ӽ����̸��Ŀ��2010��10�±������׳ơ�һ���㡱���ж����ʱ���ʳ�ú�����˸��࣬�����°�����һ���㡱�ķ��ӽṹ��ͼ��ʾ������˵����ȷ���ǣ�������
 ���ӽ����̸��Ŀ��2010��10�±������׳ơ�һ���㡱���ж����ʱ���ʳ�ú�����˸��࣬�����°�����һ���㡱�ķ��ӽṹ��ͼ��ʾ������˵����ȷ���ǣ�������
���ӽ����̸��Ŀ��2010��10�±������׳ơ�һ���㡱���ж����ʱ���ʳ�ú�����˸��࣬�����°�����һ���㡱�ķ��ӽṹ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ���л���ķ���ʽΪC7H10O3 | |
| B�� | 1mol���л����������2mol H2�����ӳɷ�Ӧ | |
| C�� | ���л����һ�ַ�����ͬ���칹���ܷ���������Ӧ | |
| D�� | ���л����ܷ���ȡ�����ӳɡ������ͻ�ԭ��Ӧ |
2����2L�ݻ�����������У�����N2+3H2?2NH3�ķ�Ӧ����ͨ��4mol H2��4mol N2��10s����H2��ʾ�ķ�Ӧ����Ϊ0.12mol/��L•s������10s��������N2�����ʵ����ǣ�������
| A�� | 1.6 mol | B�� | 2.8 mol | C�� | 3.2 mol | D�� | 3.6 mol |
6���±�ΪԪ�����ڱ���һ���֣�a��b��c��Ϊ����Ԫ�أ��ش��������⣺
��1����д������Ԫ��d3+�ĺ�������Ų�ʽ1s222s2p63s23p63d5��
��2����д��j�ĵ�����a��h�γɵĻ��������Ӧ�Ļ�ѧ����ʽCl2+H2O=HCl+HClO��
��3����Ƚ�b��e��j����Ԫ�صĵ縺���ɴ�С��˳��Cl��Al��Mg��дԪ�ط��ţ���������Ԫ�صĵ�һ�������ɴ�С��˳��Cl��Mg��Al��дԪ�ط��ţ���
��4��g��e����Ԫ�ص�����������Ӧ��ˮ����Ļ�ѧ�������ƣ���д��eԪ������������Ӧ��ˮ������a��c��h����Ԫ���γɵĻ����ﷴӦ�����ӷ���ʽAl��OH��3+OH-=AlO2-+2H2O��
��5��j��k��l����Ԫ��֮������ԭ�Ӹ�����1��1�����γɻ������Щ�������������������ЩԪ�ص��ʵ����ʣ���д��k��l�Ļ�����ĵ���ʽ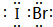 �������ɦļ�������ԭ�ӹ�����ص��̶���д���γɵĹ��ۻ��������ӡ����ۡ�����
�������ɦļ�������ԭ�ӹ�����ص��̶���д���γɵĹ��ۻ��������ӡ����ۡ�����
| a | |||||||||||||||||
| f | h | i | |||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | k | ||||||||||||||
| l | |||||||||||||||||
��2����д��j�ĵ�����a��h�γɵĻ��������Ӧ�Ļ�ѧ����ʽCl2+H2O=HCl+HClO��
��3����Ƚ�b��e��j����Ԫ�صĵ縺���ɴ�С��˳��Cl��Al��Mg��дԪ�ط��ţ���������Ԫ�صĵ�һ�������ɴ�С��˳��Cl��Mg��Al��дԪ�ط��ţ���
��4��g��e����Ԫ�ص�����������Ӧ��ˮ����Ļ�ѧ�������ƣ���д��eԪ������������Ӧ��ˮ������a��c��h����Ԫ���γɵĻ����ﷴӦ�����ӷ���ʽAl��OH��3+OH-=AlO2-+2H2O��
��5��j��k��l����Ԫ��֮������ԭ�Ӹ�����1��1�����γɻ������Щ�������������������ЩԪ�ص��ʵ����ʣ���д��k��l�Ļ�����ĵ���ʽ
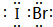 �������ɦļ�������ԭ�ӹ�����ص��̶���д���γɵĹ��ۻ��������ӡ����ۡ�����
�������ɦļ�������ԭ�ӹ�����ص��̶���д���γɵĹ��ۻ��������ӡ����ۡ�����
4���������ʵĵ���ʽ��д��ȷ���ǣ�������
| A�� | �Ȼ���  | B�� | ������̼  | ||
| C�� | ����  | D�� | �Ȼ�þ  |
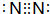 ����д��������Ԫ����ɵķ����к���4��ԭ�Ӻ���Ϊ18���ӽṹ�����ʵĻ�ѧʽH2O2��
����д��������Ԫ����ɵķ����к���4��ԭ�Ӻ���Ϊ18���ӽṹ�����ʵĻ�ѧʽH2O2��