题目内容
2.瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图,有关说法正确的是( )
| A. | 电池工作时,Na+向负极移动 | |
| B. | 通氨气的电极1作电池的正极 | |
| C. | 电子由电极2经外电路流向电极1 | |
| D. | 燃料电池的总反应为:4NH3+3O2=2N2+6H2O |
分析 A、原电池中的阳离子向正极移动;
B、在燃料电池的负极上发生燃料失电子的氧化反应,在正极上氧气发生得电子的还原反应;
C、原电池中,电子是从负极流向正极;
D、燃料电池的总反应是燃料燃烧的化学方程式.
解答 解:根据电池的工作原理示意图,知道通氧气的电极2是正极,电极1是负极;
A、原电池工作时,电解质中的阳离子向正极移动,即Na+向正极移动,故A错误;
B、在燃料电池的负极上发生燃料氨气失电子的氧化反应,所以通氨气的电极1作电池的负极,故B错误;
C、原电池中,电子是从负极电极1流向正极电极2,故C错误;
D、燃料电池的总反应是燃料燃烧的化学方程式,即4NH3+3O2=2N2+6H2O,故D正确.
故选D.
点评 燃料电池的工作原理和规律:负极上是燃料失电子的氧化反应,在正极上氧气发生得电子的还原反应.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
12.可以把6种无色液体:乙醇、苯酚、CCl4、AgNO3溶液、KOH溶液、氢硫酸区分开的试剂是( )
| A. | 新制碱性Cu(OH)2悬浊液 | B. | FeCl3溶液 | ||
| C. | BaCl2溶液 | D. | 酸性KMnO4溶液 |
13.一定量的混合气体在密闭容器中发生反应:mA(g)+nB(g)═pC(g)达到平衡后,维持温度不变,将气体体积缩小到原来的$\frac{1}{2}$,当达到新的平衡后,气体C的浓度为原平衡的1.9倍.则下列说的正确的是( )
| A. | m+n<p | B. | 平衡向正反应方向移动 | ||
| C. | m+n>p | D. | C的质量分数增加 |
17.现有H2、CO、CH4的混合气体VL,其体积比为1:1:2.当aL该混合气体完全燃烧时,所需相同条件下O2的体积为( )
| A. | $\frac{5V}{4}L$ | B. | 5VL | C. | 5aL | D. | $\frac{5a}{4}L$ |
14.下列叙述错误的是( )
| A. | 氧化铁常用作红色油漆和涂料 | |
| B. | 司母戊鼎是青铜制品 | |
| C. | 光导纤维的主要成分是硅酸盐 | |
| D. | 常温下可用铁制或铝制容器盛装浓硫酸 |
1.聚合硫酸铁(PFS)是一种重要的无机高分子絮凝剂,在工业和生活污水处理等领域具有重要应用.PFS可表示成Fex(OH)y(SO4)z(其中铁元素化合价为+3),工业上常用绿矾等原料制备,采用“一锅法”制备PFS的工艺流程如下.
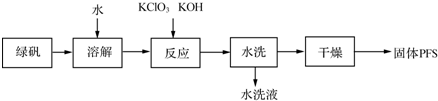
(1)从上述流程判断,水洗液中可以回收的主要物质有KCl、K2SO4.
(2)绿矾溶液与KClO3、KOH发生反应,其中还原剂与氧化剂的物质的量之比为6:1.
(3)下表是PFS的三种生产工艺所使用的原料.
试分析“一锅法”工艺的优点是未使用硫酸,不腐蚀设备,选择表中的一种方案分析其可能的缺点双氧水法:反应放热,双氧水分解(或次氯酸钠法:产生氯气,污染环境或硝酸氧化法:产生NO2等氮氧化物污染环境).
(4)在PFS的多个质量指标中,盐基度是重要的质量指标之一,盐基度定义为:盐基度=$\frac{n(O{H}^{-})}{3n(Fe)}$×100%,式中n(OH-)、n(Fe)分别表示聚合硫酸铁中OH-和Fe的物质的量.取7.51g某聚合硫酸铁溶解于稀盐酸,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀10.48g;再向上述滤液中加入足量NH3•H2O,经过滤、洗涤、干燥、灼烧得Fe2O3固体2.80g.试计算该固体聚合硫酸铁的盐基度.

(1)从上述流程判断,水洗液中可以回收的主要物质有KCl、K2SO4.
(2)绿矾溶液与KClO3、KOH发生反应,其中还原剂与氧化剂的物质的量之比为6:1.
(3)下表是PFS的三种生产工艺所使用的原料.
| 方法 | 双氧水氧化法 | 次氯酸钠氧化法 | 硝酸氧化法 |
| 原料 | 绿矾、硫酸、双氧水 | 绿矾、硫酸、次氯酸钠 | 绿矾、硫酸、浓硝酸等 |
(4)在PFS的多个质量指标中,盐基度是重要的质量指标之一,盐基度定义为:盐基度=$\frac{n(O{H}^{-})}{3n(Fe)}$×100%,式中n(OH-)、n(Fe)分别表示聚合硫酸铁中OH-和Fe的物质的量.取7.51g某聚合硫酸铁溶解于稀盐酸,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀10.48g;再向上述滤液中加入足量NH3•H2O,经过滤、洗涤、干燥、灼烧得Fe2O3固体2.80g.试计算该固体聚合硫酸铁的盐基度.
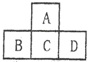 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素的原子核外共有56个电子,在周期表中的位置如图所示.E元素的最高价氧化物既能与强酸反应又能与强碱反应.请回答:
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素的原子核外共有56个电子,在周期表中的位置如图所示.E元素的最高价氧化物既能与强酸反应又能与强碱反应.请回答: ,.
,. A、B、C、D、E五种元素是周期表中前四周期的元素.只有A、B、C为金属且同周期,原子序数A<B<C.A、C核外均没有未成对电子;B原子核外有二个未成对电子和三个空轨道.D原子最外层电子数是其周期序数的三倍.E能与D形成化合物ED2,可用于自来水的消毒.
A、B、C、D、E五种元素是周期表中前四周期的元素.只有A、B、C为金属且同周期,原子序数A<B<C.A、C核外均没有未成对电子;B原子核外有二个未成对电子和三个空轨道.D原子最外层电子数是其周期序数的三倍.E能与D形成化合物ED2,可用于自来水的消毒.