题目内容
1.聚合硫酸铁(PFS)是一种重要的无机高分子絮凝剂,在工业和生活污水处理等领域具有重要应用.PFS可表示成Fex(OH)y(SO4)z(其中铁元素化合价为+3),工业上常用绿矾等原料制备,采用“一锅法”制备PFS的工艺流程如下.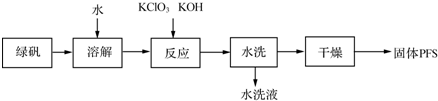
(1)从上述流程判断,水洗液中可以回收的主要物质有KCl、K2SO4.
(2)绿矾溶液与KClO3、KOH发生反应,其中还原剂与氧化剂的物质的量之比为6:1.
(3)下表是PFS的三种生产工艺所使用的原料.
| 方法 | 双氧水氧化法 | 次氯酸钠氧化法 | 硝酸氧化法 |
| 原料 | 绿矾、硫酸、双氧水 | 绿矾、硫酸、次氯酸钠 | 绿矾、硫酸、浓硝酸等 |
(4)在PFS的多个质量指标中,盐基度是重要的质量指标之一,盐基度定义为:盐基度=$\frac{n(O{H}^{-})}{3n(Fe)}$×100%,式中n(OH-)、n(Fe)分别表示聚合硫酸铁中OH-和Fe的物质的量.取7.51g某聚合硫酸铁溶解于稀盐酸,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀10.48g;再向上述滤液中加入足量NH3•H2O,经过滤、洗涤、干燥、灼烧得Fe2O3固体2.80g.试计算该固体聚合硫酸铁的盐基度.
分析 绿矾用水溶解,再加入次氯酸钾、KOH,氯酸根离子具有氧化性,亚铁离子具有还原性,发生反应:6FeSO4+KClO3+12KOH═6Fe(OH)3↓+KCl+6K2SO4+6H2O,水洗、干燥得到PFS,水洗后溶液中含有KCl、K2SO4.
(1)水洗后溶液中含有KCl、K2SO4;
(2)还原剂为FeSO4,氧化剂是KClO3,结合反应方程式判断还原剂、氧化剂物质的量的之比;
(3)“一锅法”未使用硫酸,不腐蚀设备;双氧水法:反应放热,双氧水分解;次氯酸钠法:产生氯气,污染环境;硝酸氧化法:产生NO2等氮氧化物污染环境;
(4)根据Fe元素守恒计算n(Fe)=2n(Fe2O3),白色沉淀10.48g为BaSO4,根据n=$\frac{m}{M}$计算n(SO42-),再根据电荷守恒计算n(OH-),再根据盐基度定义式计算.
解答 解:绿矾用水溶解,再加入次氯酸钾、KOH,氯酸根离子具有氧化性,亚铁离子具有还原性,发生反应:6FeSO4+KClO3+12KOH═6Fe(OH)3↓+KCl+6K2SO4+6H2O,水洗、干燥得到PFS,水洗后溶液中含有KCl、K2SO4.
(1)水洗后溶液中含有KCl、K2SO4,以回收的主要物质有:KCl、K2SO4,
故答案为:KCl、K2SO4;
(2)发生反应:发生反应:6FeSO4+KClO3+12KOH═6Fe(OH)3↓+KCl+6K2SO4+6H2O,还原剂为FeSO4,氧化剂是KClO3,还原剂、氧化剂物质的量的之比为6:1,
故答案为:6:1;
(3)“一锅法”未使用硫酸,不腐蚀设备;双氧水法:反应放热,双氧水分解;次氯酸钠法:产生氯气,污染环境;硝酸氧化法:产生NO2等氮氧化物污染环境;
故答案为:未使用硫酸,不腐蚀设备;双氧水法:反应放热,双氧水分解(或次氯酸钠法:产生氯气,污染环境或硝酸氧化法:产生NO2等氮氧化物污染环境);
(4)根据Fe元素守恒:n(Fe)=2n(Fe2O3)=$\frac{2.8g}{160g/mol}$×2=0.035 mol,
白色沉淀10.48g为BaSO4,n(SO42-)=n(BaSO4)=$\frac{10.48g}{233g/mol}$=0.045mol,
根据电荷守恒:n(OH-)=3×n(Fe)-2×n(SO42-)=3×0.035mol-2×0.045mol=0.015mol,则盐基度=$\frac{0.015mol}{0.035mol×3}$×100%=14.29%,
答:该固体聚合硫酸铁的盐基度是14.29%.
点评 本题综合考查化学工艺流程、实验制备方案评价、化学计算等,是对学生综合能力的考查,明确反应原理是根据,难度中等.

 将一定质量的钠、钾分别投入到盛有相同浓度和体积的盐酸的两个烧杯中,产生的气体随时间变化曲线如图所示,则下列说法正确的是( )
将一定质量的钠、钾分别投入到盛有相同浓度和体积的盐酸的两个烧杯中,产生的气体随时间变化曲线如图所示,则下列说法正确的是( )| A. | 投入的Na、K的质量一定相等 | |
| B. | 投入的Na的质量小于K的质量 | |
| C. | 曲线A表示Na与盐酸反应,曲线B表示K与盐酸反应 | |
| D. | 该实验能证明K的金属性小于Na的金属性 |

| A. | 电池工作时,Na+向负极移动 | |
| B. | 通氨气的电极1作电池的正极 | |
| C. | 电子由电极2经外电路流向电极1 | |
| D. | 燃料电池的总反应为:4NH3+3O2=2N2+6H2O |
| A. | 加热Al2O3 | B. | 加热HgO | C. | 电解熔融NaCl | D. | 铝粉和Fe2O3共热 |
| A. | 同一元素各核素的质量数不同,但它们的化学性质几乎完全相同 | |
| B. | 任何元素的原子都是由核外电子和核内中子、质子构成的 | |
| C. | 钠原子失去一个电子后,它的电子数与氖原子相同,变成10e-微粒 | |
| D. | ${\;}_{18}^{40}$Ar、${\;}_{19}^{40}$K、${\;}_{20}^{40}$Ca的质量数相同,所以它们互为同位素 |
(1)在高温下一氧化碳可将二氧化硫还原为单质硫.已知;
C(s)+O2(g)=CO2(g);△H1=-393.5kJ•mol-1
CO2(g)+C(s)=2CO(g);△H2=+172.5kJ•mol-1
S(s)+O2(g)=SO2(g);△H3=-296.0kJ•mol-1
则2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-270kJ•mol-1
(2)以 CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为CnH2nOn-4ne-+nH2O=nCO2+4nH+
(3)工业上一般采用CO与H2反应合成可再生能源甲醇,反应如下:CO(g)+2H2(g)?CH3OH(g)
①某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.2mol•L-1,则CO的转化率为80%.
②合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,通过反应进行甲醇合成,T1℃下此反应的平衡常数为160,
此温度下,在密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol•L-1) | 0.2 | 0.1 | 0.4 |
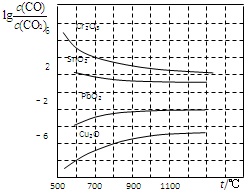
(4)金属氧化物被一氧化碳还原生成金属单质和二氧化碳.如图是四种金属氧化物被一氧化碳还原时lg[c(CO)/c(CO2)]与温度(t)的关系曲线图.800℃时,其中最易被还原的金属氧化物是Cu2O(填化学式),该反应的平衡常数数值(K)等于106.
| A. | 仅用酸性高锰酸钾溶液可区分苯和甲苯 | |
| B. | 仅用氯化铁溶液可区分苯酚稀溶液和甘油 | |
| C. | 仅用硝酸银溶液可验证卤代烃中卤原子的种类 | |
| D. | 仅用溴的四氯化碳溶液可区别液态的植物油和动物油 |
| 实验序号 | 温度T/℃ | A溶液 | B溶液 |
| ① | 30 | 20mL0.1mol•L-1H2C2O4溶液 | 30mL0.01mol•L-1KMnO4溶液 |
| ② | 20 | 20mL0.1mol•L-1H2S2O4溶液 | 30mL0.01mol•L-1KMnO4溶液 |
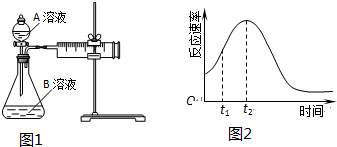
(2)该实验探究的是浓度因素对化学反应速率的影响.相同时间内针筒中所得CO2的体积大小关系是:①<②(填:>、<、=).
(3)若实验①在2min末收集了2.24mL CO2(标准状况下),则在2min末,c(MnO4-)=0.0056mol/L.
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率.
(5)小组同学发现反应速率总是如图2,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+(或MnSO4)是反应的催化剂②该反应放热.
 硫酸钠与工农业生产、生活紧密相关,工业硫酸钠大多采用侯氏制碱法制取.
硫酸钠与工农业生产、生活紧密相关,工业硫酸钠大多采用侯氏制碱法制取.