题目内容
【题目】实验测定某硫代硫酸钠晶体(Na2S2O3·5H2O,M=248 g·mol-1)样品纯度的过程为:称取1.5000 g样品,配成100 mL溶液。取0.01mol ·L-1的K2Cr2O7标准溶液20.00 mL,硫酸酸化后加入过量的KI。充分反应后,以淀粉作指示剂,用硫代硫酸钠溶液滴定产生的I2,终点时消耗溶液20.00 mL。样品中所含硫代硫酸钠晶体的质量分数为(杂质不参与反应,反应过程中的物质转化关系为K2Cr2O7![]() I2
I2![]() S4O
S4O![]() )
)
A.99.20%B.96.72%C.94.24%D.91.76%
【答案】A
【解析】
0.01mol ·L-1的K2Cr2O7标准溶液20.00 mL中含有K2Cr2O7的物质的量为0.01mol ·L-1×0.02L=2×10-4mol,由K2Cr2O7![]() I2
I2![]() S4O
S4O![]() 根据电子守恒可知K2Cr2O7~~~3I2~~~6S2O
根据电子守恒可知K2Cr2O7~~~3I2~~~6S2O![]() ,则20.00 mL硫代硫酸钠溶液中含有硫代硫酸钠的物质的量为2×10-4mol×6=1.2×10-3mol,样品中所含硫代硫酸钠晶体的质量分数为
,则20.00 mL硫代硫酸钠溶液中含有硫代硫酸钠的物质的量为2×10-4mol×6=1.2×10-3mol,样品中所含硫代硫酸钠晶体的质量分数为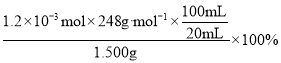 =99.20%,故答案为A。
=99.20%,故答案为A。

 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(实验原理)2KMnO4 + 5H2C2O4 + 3H2SO4= K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
(实验内容及记录)
实验编号 | 室温下,试管中所加试剂及其用量 / mL | 室温下溶液颜色褪至无色所需时间 / min | |||
0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05mol/L KMnO4溶液 | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | V1 | 2.7 |
3 | 1.0 | V2 | 2.0 | 3.0 | 3.9 |
请回答:(1)表中V1=___________,V2=___________。
(2)根据上表中的实验数据,可以得到的结论是_____________________________。
(3)利用实验1中数据计算,若用KMnO4的浓度变化表示的反应速率为:υ(KMnO4)= ________________________。
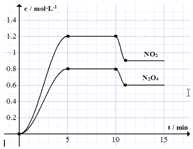
(4)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。(忽略反应过程中温度变化)
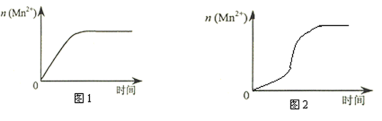
①该小组同学提出的假设是_______________________________________。
②请你帮助该小组同学完成实验方案。
实验编号 | 室温下,试管中所加试剂及其用量 / mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 / min | |||
0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05 mol/L KMnO4溶液 | |||
4 | 3.0 | 2.0 | 2.0 | 3.0 | A | t |
表中加入的固体A是_______________。(写化学式)
③若该小组同学提出的假设成立,应观察到的现象是____________
(5)工业上可用电解K2MnO4溶液的方法制取KMnO4,则电解时,阳极发生的电极反应式为____________________________________。