题目内容
【题目】1-氯丙烷和2-氯丙烷分别与NaOH乙醇溶液共热的反应,下列有关说法不正确的是( )
A. 产物相同B. 碳氢键断裂的位置相同
C. 反应类型相同D. 1-氯丙烷和2-氯丙烷都能与NaOH水溶液共热的发生反应
【答案】B
【解析】
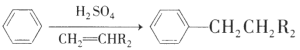
卤代烃在氢氧化钠的醇溶液中发生消去反应,反应时卤素原子与相邻的碳上的一个氢同时脱去,形成碳碳双键。1-氯丙烷发生消去反应的方程式为CH3CH2CH2Cl+NaOH![]() CH3CH=CH2↑+NaCl+H2O,2-氯丙烷发生消去反应的方程式为CH3CHClCH3+NaOH
CH3CH=CH2↑+NaCl+H2O,2-氯丙烷发生消去反应的方程式为CH3CHClCH3+NaOH ![]() CH3CH=CH2↑+NaCl+H2O。
CH3CH=CH2↑+NaCl+H2O。
A项、1-氯丙烷和2-氯丙烷的消去产物是相同的,都是丙烯,故A正确;
B项、1-氯丙烷发生消去反应时断1号C的C-Cl键,2-氯丙烷发生消去反应时断2号C的C-Cl键,故B错误;
C项、1-氯丙烷和2-氯丙烷在氢氧化钠的醇溶液中均发生消去反应,故C正确;
D项、1-氯丙烷和2-氯丙烷都在NaOH水溶液中共热发生水解反应,分别生成1—丙醇和2—丙醇,故D正确。
故选B。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案【题目】表为元素周期表的一部分,请回答有关问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ |
(1)表中最活泼的金属是___________,非金属性最强的元素是____________。(填写元素符号,下同)
(2)表中能形成两性氢氧化物的元素是_______________,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物对应水化物反应的化学方程式:___________、___________。
(3)⑨最高价氧化物对应水化物的电子式______________。
(4)利用下图装置来验证同主族元素非金属性的变化规律:
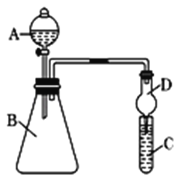
要证明非金属性:C>Si,在A中加盐酸,B中加CaCO3,C中加Na2SiO3溶液,应在B、D之间增加一个盛有足量____(选填下列字母:A 浓盐酸 、B 浓NaOH溶液、C 饱和Na2CO3溶液 、D 饱和NaHCO3溶液)的洗气装置.改进后C中发生反应的化学方程式是_____.