题目内容
15. 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:CH3CH=CH2+CO+H2$\stackrel{一定条件}{→}$CH3CH2CH2CHO$\stackrel{H_{2},Ni,加热}{→}$2CH2CH2OH
CO的制备原理:HCOOH $\stackrel{浓硫酸、加热}{→}$ CO↑+H2O
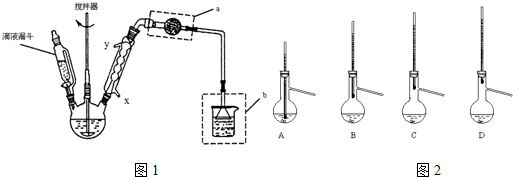
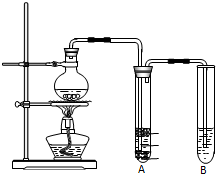
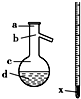
并设计出原料气的制备装置(如图)
请填写下列空白:
(1)若用以上装置制备干燥纯净的CO,装置中a和b的作用分别是恒压,防倒吸;c和d中盛装的试剂分别是NaOH溶液,浓硫酸.
(2)用2-丙醇制丙烯时,还产生少量SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体(每次试剂只能用一次),混合气体通过试剂的顺序是④⑤①②③(或④⑤①③②)(填序号).
①饱和Na2SO3溶液 ②酸性KMnO4溶液 ③石灰水
④无水CuSO4 ⑤品红溶液
(3)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是b.
a.低温、高压、催化剂
b.适当的温度、高压、催化剂
c.常温、常压、催化剂
d.适当的温度、常压、催化剂
(4)正丁醛经催化剂加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,该小组查阅文献得知:①R-CHO+NaHSO3(饱和)→RCH(OH)SO3Na↓;②沸点:乙醚34℃,1-丁醇118℃,并设计出如下提纯路线:
粗品$→_{操作1}^{试剂1}$滤液$→_{操作2}^{乙醚}$$\underset{→}{分液}$有机层$→_{过滤}^{干燥剂}$1-丁醇,乙醚$\underset{→}{操作3}$纯品
试剂1为饱和NaHSO3溶液,操作1为过滤,操作2为萃取,操作3为蒸馏.
分析 (1)甲酸在浓硫酸的作用下通过加热脱水生成CO,由于甲酸易挥发,产生的CO中必然会混有甲酸,所以在收集之前需要除去甲酸,可以利用NaOH溶液吸收甲酸.甲酸易溶于水,所以必需防止液体倒流,即b的作用是防止倒吸,最后通过浓硫酸干燥CO.为了使产生的气体能顺利的从发生装置中排出,就必需保持压强一致,因此a的作用是保持恒压;
(2)用无水硫酸铜检验水,用品红检验二氧化硫,并用酸性高锰酸钾除去二氧化硫,最后用石灰水检验二氧化碳;
(3)题给合成正丁醛的反应为气体体积减小的放热反应,为增大反应速率和提高原料气的转化率;
(4)饱和NaHSO3溶液形成沉淀,然后通过过滤即可除去;加入乙醚的目的是萃取溶液中的1-丁醇,1-丁醇和乙醚的沸点相差很大,因此可以利用蒸馏将其分离开.
解答 解:(1)甲酸在浓硫酸的作用下通过加热脱水即生成CO,由于甲酸易挥发,产生的CO中必然会混有甲酸,所以在收集之前需要除去甲酸,可以利用NaOH溶液吸收甲酸.甲酸易溶于水,所以必需防止液体倒流,即b的作用是防止倒吸,最后通过浓硫酸干燥CO.为了使产生的气体能顺利的从发生装置中排出,就必需保持压强一致,因此a的作用是保持恒压,
故答案为:保持恒压;防倒吸; NaOH溶液;浓硫酸;
(2)检验丙烯可以用酸性KMnO4溶液,检验SO2可以用酸性KMnO4溶液褪色、品红溶液或石灰水,检验CO2可以石灰水,检验水蒸气可以无水CuSO4,所以在检验这四种气体必需考虑试剂的选择和顺序.只要通过溶液,就会产生水蒸气,因此先检验水蒸气;然后检验SO2并在检验之后除去SO2,除SO2可以用饱和Na2SO3溶液,最后检验CO2和丙烯,因此顺序为④⑤①②③(或④⑤①③②),
故答案为:④⑤①②③(或④⑤①③②);
(3)由于反应是一个体积减小的可逆反应,所以采用高压,有利于增大反应速率和提高原料气的转化率;正向反应是放热反应,虽然低温有利于提高原料气的转化率,但不利于增大反应速率,因此要采用适当的温度;催化剂不能提高原料气的转化率,但有利于增大反应速率,缩短到达平衡所需要的时间,故正确所选项是b;
故答案为:b;
(4)粗品中含有正丁醛,根据所给的信息利用饱和NaHSO3溶液形成沉淀,然后通过过滤即可除去;由于饱和NaHSO3溶液是过量的,所以加入乙醚的目的是萃取溶液中的1-丁醇.因为1-丁醇和乙醚的沸点相差很大,因此可以利用蒸馏将其分离开,
故答案为:饱和NaHSO3溶液;过滤;萃取;蒸馏.
点评 本题考查有机物合成方案的设计,题目难度中等,综合性较强,答题时注意把握物质的分离、提纯方法,把握物质的性质的异同是解答该题的关键.

| A. | 3SO2+2NO3-+2H2O═2NO↑+4H++3SO42- | |
| B. | 3SO2+Ba2++2NO3-+2H2O═BaSO4↓+2NO↑+4H++SO42- | |
| C. | 6SO2+Ba2++4NO3-+4H2O═BaSO4↓+4NO↑+8H++5SO42- | |
| D. | 3SO2+3Ba2++2NO3-+2H2O═3BaSO4↓+2NO↑+4H+ |
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向沸水中滴加少量饱和氯化铁溶液,加热至溶液呈红褐色,用激光笔照射 | 有丁达尔效应 | 红褐色液体为胶体 |
| B | 向溶液X中加入NaHCO3粉末 | 产生无色气体 | X一定属于酸 |
| C | 向淀粉NaI溶液中加入氯水 | 溶液变蓝 | 氧化性:Cl2>I2 |
| D | 将气体X分别通入溴水和酸性高锰酸钾溶液 | 两溶液均褪色 | X可能是SO2 |
| A. | A | B. | B | C. | C | D. | D |

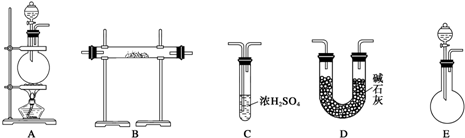
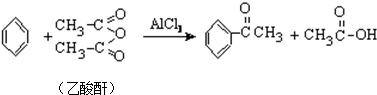
 实验室中用苯甲醛制备苯甲醇和苯甲酸,已知反应原理:2HCHO+KOH-→CH3OH+HCOOK
实验室中用苯甲醛制备苯甲醇和苯甲酸,已知反应原理:2HCHO+KOH-→CH3OH+HCOOK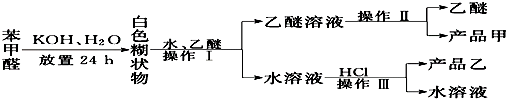
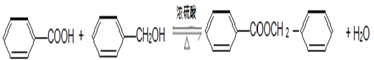 ,实验室在收集此特殊香味的物质时常用饱和Na2CO3溶液 (填试剂名称)除去其中的杂质,且便于其分层析出.
,实验室在收集此特殊香味的物质时常用饱和Na2CO3溶液 (填试剂名称)除去其中的杂质,且便于其分层析出.