题目内容
1.金属铝为银白色金属,具有良好的导电性和导热性;在地壳中铝元素的含量处第3位.铝原子最外层有3电子,在化合物中常表现+3价,在金属活动性顺序中,铝属于活泼金属,但由于在空气中和氧气反应使铝表面形成一层致密的氧化铝从而使铝很难和其他物质反应,有关反应的化学方程式为2Al+3O2=2Al2O3.分析 铝具有金属光泽,具有金属的通性,在地壳中铝元素的含量处第3位,铝为13号元素,最外层为3个,表现+3价,金属性活泼,在空气容易形成致密的氧化物,因此抗腐蚀性能很好,据此分析进行解答.
解答 解:铝具有金属光泽,为银白色金属,具有良好的导电性,常用作电线成分,具有良好的导热性,常用作炊具,在地壳中铝元素的含量处第3位,铝原子的原子结构示意图为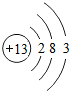 ,元素的正化合价数等于其原子的最外层电子数,可知铝元素常见化合价为+3;铝比铁活泼,但是铝制品比铁制品耐腐蚀,原因是:铝在常温下与空气中的氧气发生化学反应,使铝的表面生成了一层致密的氧化铝薄膜从而阻止了内部的铝进一步氧化,反应为:2Al+3O2=2Al2O3,
,元素的正化合价数等于其原子的最外层电子数,可知铝元素常见化合价为+3;铝比铁活泼,但是铝制品比铁制品耐腐蚀,原因是:铝在常温下与空气中的氧气发生化学反应,使铝的表面生成了一层致密的氧化铝薄膜从而阻止了内部的铝进一步氧化,反应为:2Al+3O2=2Al2O3,
故答案为:银白;导电;导热;3;3;+3;活泼;氧化铝;难;2Al+3O2=2Al2O3.
点评 本题主要考查金属铝的性质和用途等方面的知识,可以依据已有的知识结合金属活动性顺序的应用以及原子结构分析,从而培养学生对有关知识的应用,题目难度不大.

练习册系列答案
相关题目
11.下列物质中锰元素的化合价最高的是( )
| A. | MnO2 | B. | MnCl2 | C. | K2MnO4 | D. | KMnO4 |
12.等体积、等物质的量浓度的盐酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为3:4,则甲、乙两烧杯中的反应情况可能分别是( )
| A. | 甲、乙中都是铝过量 | B. | 甲中铝过量,乙中碱过量 | ||
| C. | 甲中酸过量,乙中铝过量 | D. | 甲、乙中都是铝不足 |
9.物质的量浓度相同的下列物质的水溶液,H+浓度最小的是( )
| A. | Na2C03 | B. | HCl | C. | Na2S04 | D. | KN03 |
16.物质的量浓度相同的NaCl溶液和NaClO溶液中,下列关系中正确的是( )
| A. | NaCl溶液中离子的总浓度和NaClO溶液中离子的总浓度相等 | |
| B. | NaCl溶液中离子的总浓度大于NaClO溶液中离子的总浓度 | |
| C. | NaCl溶液中离子的总浓度小于NaClO溶液中离子的总浓度 | |
| D. | NaCl溶液的pH大于NaClO溶液的pH |
6.能正确表示下列反应的离子(或化学)方程式是 ( )
| A. | 金属Al溶于稀硝酸中:2Al+6H+═2Al3++3H2↑ | |
| B. | CuH在足量C12中燃烧:2CuH+2Cl2$\frac{\underline{\;点燃\;}}{\;}$2CuCl2+H2 | |
| C. | 向复盐NH4Al(S04)2溶液中加入Ba(0H)2至沉淀质量最大:NH4++Al3++4OH-+2SO42-═NH3•H2O+Al(OH)3↓+2BaSO4↓ | |
| D. | 向饱和NaHSO3溶液中加入FeC13溶液:S032-+2Fe3++H20═S042-+2Fe2++2H+ |

 .
.  ;
;
 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线: