题目内容
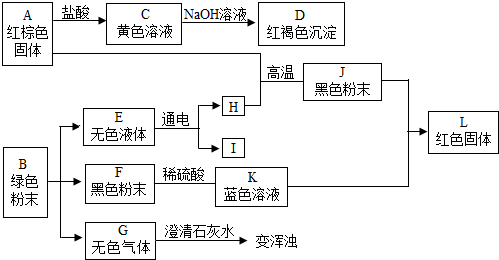
6.硫铁矿烧渣(主要成分Fe2O3、Fe3O4、FeO、SiO2等)是工业生产硫酸的废渣,利用硫铁矿烧渣制备铁红等产品的流程如图所示
回答下列问题:
(1)若焙烧时还原剂碳燃烧产生的气体能将铁的多种氧化物还原成铁单质,则该气体与Fe2O3反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)酸浸时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因用离子方程式表示为4Fe2++O2+4H+=4Fe3++2H2O.
(3)加碳酸氢铵合成时反应温度一般需控制在35℃以下,其目的是防止NH4HCO3分解.
(4)若产品Ⅱ的主要成分是K2SO4,则试剂X为KCl,反应的离子方程式为2K++SO42-=K2SO4↓.
(5)空气中煅烧FeCO3生成产品Ⅰ的化学反应方程式为4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2.
(6)检验产品II中是否含有氯化物杂质的实验操作是:取少量产品Ⅱ于试管中配成溶液,滴加过量Ba(NO3)2溶液,过滤后向滤液滴加AgNO3溶液滴加过量Ba(NO3)2溶液,过滤后向滤液滴加AgNO3溶液.
分析 Fe2O3、Fe3O4、FeO与还原剂反应生成铁,铁和稀硫酸反应生成硫酸亚铁和氢气,过滤时用到的仪器有铁架台、漏斗、烧杯、玻璃棒等,所以滤液中的主要溶质是硫酸亚铁;硫酸亚铁与碳酸氢铵反应得到碳酸亚铁和硫酸铵,实验室进行煅烧操作所需仪器有酒精灯、泥三角、三脚架、玻璃棒、坩埚、坩埚钳;碳酸亚铁与氧气反应生成了氧化铁和二氧化碳;硫酸铵与氯化钾反应生成硫酸钾和氯化铵,根据硫酸钾的溶解度随温度变化不大,可用蒸发结晶、趁热过滤、洗涤、干燥得到硫酸钾,检验产品II中是否含有氯化物杂质需先除去SO4,再检验Cl-,以此解答该题,
(1)若焙烧时还原剂碳燃烧产生的气体为CO,与氧化铁反应生成铁和二氧化碳气体;
(2)溶液中Fe2+具有还原性,可被空气中氧气氧化含量将下降;
(3)碳酸氢铵不稳定,加热易分解;
(4)流程图可以看出酸浸、过滤后滤液中的溶质主要是硫酸亚铁,硫酸亚铁和碳酸氢铵反应生成碳酸亚铁和硫酸铵,过滤后反应Ⅱ中硫酸铵与X反应生成硫酸钾和氯化铵,因此加入的X应为氯化钾,过滤得到硫酸钾,说明硫酸钾溶解度小;
(5)碳酸亚铁与氧气反应生成了氧化铁和二氧化碳;
(6)因检验产品II中是否含有氯化物杂质需先除去SO4,再检验Cl-.
解答 解:(1)若焙烧时还原剂碳燃烧产生的气体为CO,与氧化铁反应生成铁和二氧化碳气体,方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,
故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)具有还原性,可被空气中氧气氧化,方程式为4Fe2++O2+4H+=4Fe3++2H2O,
故答案为:4Fe2++O2+4H+=4Fe3++2H2O;
(3)碳酸氢铵不稳定,加热易分解,应在温度较低的情况下加热,
故答案为:防止碳酸氢铵分解;
(4)由流程图可以看出酸浸、过滤后滤液中的溶质主要是硫酸亚铁,硫酸亚铁和碳酸氢铵反应生成碳酸亚铁和硫酸铵,过滤后反应Ⅱ中硫酸铵与X反应生成硫酸钾和氯化铵,因此加入的X应为氯化钾,要过滤得到硫酸钾,说明在此条件下硫酸钾的溶解度小于氯化铵的溶解度,反应的离子方程式为:2K++SO42-=K2SO4↓,
故答案为:KCl;2K++SO42-=K2SO4↓;
(5)碳酸亚铁与氧气反应生成了氧化铁和二氧化碳,4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2,
故答案为:4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2;
(6)因检验产品II中是否含有氯化物杂质需先除去SO4,再检验Cl-,所以滴加过量Ba(NO3)2溶液,过滤后向滤液滴加AgNO3溶液,
故答案为:滴加过量Ba(NO3)2溶液,过滤后向滤液滴加AgNO3溶液.
点评 本题综合考查物质的分离、提纯以及制备,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握实验的目的和原理,难度中等.

 名校课堂系列答案
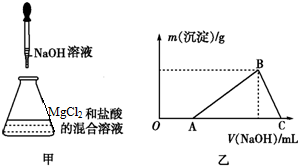
名校课堂系列答案| A. | 甲、乙中都是铝过量 | B. | 甲中铝过量,乙中碱过量 | ||
| C. | 甲中酸过量,乙中铝过量 | D. | 甲、乙中都是铝不足 |
(1)实验室中通常用NaOH溶液进行洗气和提纯,当用100mL 3mol•L-1的NaOH溶液吸收标准状况下4.48L CO2时,所得溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
(2)常温下,向一定体积的0.1mol•L-1的醋酸溶液中加水稀释后,下列说法正确的是CD.
A.溶液中导电粒子的数目减少 B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中
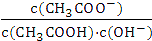 不变 D.溶液中
不变 D.溶液中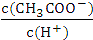 减小
减小(3)常温下将0.15mol•L-1的稀硫酸V1mL与0.1mol•L-1的NaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=1:1(溶液体积的变化忽略不计).
(4)常温下,浓度均为0.1mol•L-1的下列五种溶液的pH如表所示:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCNB.HClO C.H2CO3D.CH3COOH
②根据以上数据,判断下列反应可以成立的是AB.
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO D.NaHCO3+HCN=NaCN+H2O+CO2↑
(5)几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
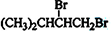 .
. 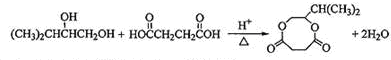 ;
;
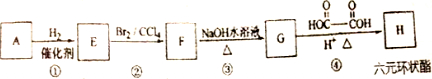
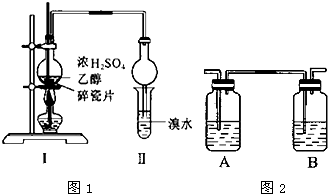 l,2二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.189cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可用下列反应制备1,2二溴乙烷.
l,2二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.189cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可用下列反应制备1,2二溴乙烷. 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线: