题目内容
2.某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种.为确认其组成,某同学取一定量该气体按下图所示装置进行实验(假设每步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,④中增重2.2g.下列关于气体X成分的分析中,错误的是( )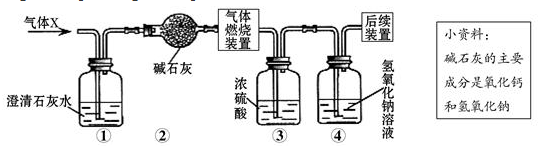
| A. | 一定没有二氧化碳 | B. | 可能含有甲烷和氢气 | ||
| C. | 可能只有甲烷 | D. | 可能含有氢气和一氧化碳 |
分析 根据各个装置的作用进行分析,①装置可以检验是否含有二氧化碳,碱石灰能吸收水分和酸性气体,浓硫酸能吸收水,氢氧化钠溶液吸收二氧化碳,装置①中无明显变化,排除了二氧化碳;装置③增重了1.8g,说明生成水1.8g,装置④增重2.2g,说明生成二氧化碳2.2g,根据水和二氧化碳的质量可以计算出C、H元素的质量比,从而确定气体X的组成.
解答 解:A、气体通过装置①中无明显变化,说明一定不含有二氧化碳,故A正确;
B、气体燃烧后,装置③增重1.8g,说明生成水为1.8g,H元素的质量为:1.8×$\frac{2}{18}$=0.2g;④中增重2.2g,说明生成二氧化碳气体2.2g,C元素的质量为2.2×$\frac{12}{44}$=0.6g,气体X中C:H=0.6:0.2=3:1,甲烷中C:H=12:4=3:1,故X的组成可能是只有甲烷,可能含有氢气和CO,可能同时含有甲烷、CO和氢气,但不可能只有甲烷和氢气,故B错误;
C、依据B的分析可知,可能只有甲烷,故C正确;
D、依据B的分析,可以是CO和氢气的混合气体,故D正确,
故选B.
点评 本题主要考查的是常见气体的检验,依据各种气体的性质以及元素组成进行分析是解决本题的关键,有一定难度.

练习册系列答案
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
13.分某学习小组在研究水处理问题时,将一定量NaClO溶液与FeSO4溶液相混合,得到含有大量悬浮物的混合液.请完成对反应物剩余情况的探究.
(1)提出合理假设:
假设1:FeSO4有剩余;
假设2:NaClO有剩余;
假设3:NaClO和FeSO4都无剩余
(2)样品初步处理:取少量混合液于试管中,滴加足量稀硫酸得到澄清溶液.此澄清溶液中肯定含有的金属阳离子是Na+,Fe3+
(3)设计后续实验方案验证假设.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:3mol.L-1 H2SO4,0.01mol•L-1 KMnO4,20% KSCN、3% H2O2,淀粉-KI溶液、紫色石蕊溶液.
(1)提出合理假设:
假设1:FeSO4有剩余;
假设2:NaClO有剩余;
假设3:NaClO和FeSO4都无剩余
(2)样品初步处理:取少量混合液于试管中,滴加足量稀硫酸得到澄清溶液.此澄清溶液中肯定含有的金属阳离子是Na+,Fe3+
| 实验步骤 | 预期现象和结论 | |
| 步骤1 | 将上述澄清溶液分置于A、B试管中. | |
| 步骤2 | ||
| 步骤3 | ||
10.已知:将C12通入适量NaOH溶液,产物中可能有NaCl、NaClO、NaClO3,且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$的值仅与温度高低有关.当n(NaOH)=6amol时,下列有关说法正确的是( )
| A. | 改变温度,反应中转移电子的物质的量n的范围:3amol≤n≤5amol | |
| B. | 改变温度,产物中NaCl的最小理论产量为4amol | |
| C. | 参加反应的氯气的物质的量3amol | |
| D. | 某温度下,若反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=6,则溶液中$\frac{c(C{l}^{-})}{c(C{O}_{3}^{-})}=\frac{1}{2}$ |
17.某粒子的结构示意图为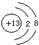 ,下列说法中不正确的是( )
,下列说法中不正确的是( )
 ,下列说法中不正确的是( )
,下列说法中不正确的是( )| A. | 该元素原子的原子核外有2个电子层 | |
| B. | 该元素是一种金属元素 | |
| C. | 该粒子是阳离子 | |
| D. | 该粒子具有稳定结构 |
14.现有0.2 mol•L-1的KHCO3溶液和0.1 mol•L-1的NaOH溶液,将两溶液等体积混合,下列说法正确的是( )
| A. | 3c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) | |
| B. | 2c(Na+)=c(HCO3-)+2c(CO32-)+c(H2CO3) | |
| C. | c(K+)>c(Na+)>c(HCO3-)+c(CO32-)>c(OH-)>c(H+) | |
| D. | c(OH-)+c(CO32-)=c(H+)+c(H2CO3)+0.1 mol•L-1 |
11.下列括号中对日常生活的变化判断正确的是( )
| A. | 嘴嚼米饭时有甜味(化学变化) | |
| B. | 玻璃窗破裂(化学变化) | |
| C. | 二氧化碳使澄清的石灰水变浑浊(物理变化) | |
| D. | 纯净物加热后变为混合物(物理变化) |
12.反应N2+3H2?2NH3,开始时N2的浓度为3mol•L-1,H2的浓度为5mol•L-1,3min后测得NH3浓度为0.6mol•L-1,则此时间内,下列反应速率表示正确的是( )
| A. | v(NH3)=0.2 mol•L-1•s-1 | B. | v(N2)=1.0 mol•L-1•min-1 | ||
| C. | v(H2)=1.67 mol•L-1•min-1 | D. | v(H2)=0.3 mol•L-1•min-1 |