题目内容
【题目】下列说法正确的是 ( )
A.氢气的燃烧热为 △H =-285.5 kJ·mol-1,则电解水的热化学方程式为2H2O(1)![]() 2H2(g)+O2(g) △H =+285.5 kJ·mol-1
2H2(g)+O2(g) △H =+285.5 kJ·mol-1
B.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量,则Fe(s)+S(s) ===FeS(s) △H =-95.6 kJ·mol-l
C.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2 (g)+3H2 (g) ![]() 2NH3 (g)△H =-38.6 kJ·mol-l
2NH3 (g)△H =-38.6 kJ·mol-l
D.相同条件下,在两个相同的恒容密闭容器中,1 mol N2和3 mol H2反应放出的热量与2 mol NH3分解吸收的热量一定一样多
【答案】B
【解析】
A.氢气的燃烧热指的是1mol氢气完全燃烧生成液态水时放出的热量,故电解水的热化学方程式为2H2O(1)![]() 2H2(g)+O2(g) △H =+571kJ·mol-1,A项错误;
2H2(g)+O2(g) △H =+571kJ·mol-1,A项错误;
B.11.2 g 铁粉即0.2mol,9.6 g硫粉即0.3mol,铁粉可完全反应,当0.2mol铁粉完全反应生成硫化亚铁时,放出19.12 kJ热量,则1mol 铁粉完全反应放出95.6 kJ热量,B项正确;
C.合成氨是可逆反应,0.5mol![]() (g)不可能完全转化为生成物,但ΔH描述的是完全反应的热效应,C项错误;
(g)不可能完全转化为生成物,但ΔH描述的是完全反应的热效应,C项错误;
D.相同条件下,在两个相同的恒容密闭容器中,1 mol![]() (g)和3mol
(g)和3mol![]() (g)反应与2mol
(g)反应与2mol![]() 分解的转化率不同,放出的热量不一样多,D项错误;
分解的转化率不同,放出的热量不一样多,D项错误;
答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
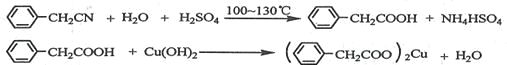
制备苯乙酸的装置示意图如下(加热和夹持装置等略):
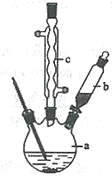
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
__________________________。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是_____________________;仪器c的名称是______________,其作用是___________________________________________。
反应结束后加适量冷水,再分离出苯乙酸粗品。加人冷水的目的是____________。下列仪器中可用于分离苯乙酸粗品的是________________(填标号)。
A.分液漏斗 | B.漏斗 | C.烧杯 | D.直形冷凝管E.玻璃棒 |
(3)提纯粗苯乙酸的方法是_____________,最终得到44 g纯品,则苯乙酸的产率是________。
(4)用CuCl2 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是____________________________________________。
(5)将苯乙酸加人到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是___________________。
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2 L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4 s内A的平均反应速率v(A)=0.005mol/(L·s)。下列说法正确的是
A.4 s时c(B)为0.76mol/L
B.830℃达平衡时,A的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为0.4
A(g)+B(g)的平衡常数的值为0.4