题目内容
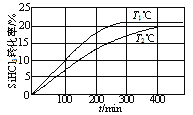
【题目】向体积均为2 L的两个恒容密闭容器中分别充入1molSiHCl3,维持容器的温度分别为T1℃和T2℃不变,发生反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g) ΔH1=a kJ·mol1。反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
SiH2Cl2(g)+SiCl4(g) ΔH1=a kJ·mol1。反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
A.T1>T2
B.T1℃时,0~100min反应的平均速率v(SiHCl3)=0.001mol·(L·min)-1
C.T2℃时,反应的平衡常数:K=1/64
D.T2℃时,使用合适的催化剂,可使SiHCl3的平衡转化率与T1℃时相同
【答案】AC
【解析】
A. “先拐先平数值大”,升高温度,化学反应速率会增大,达到平衡的时间会缩短,图中可看出T1>T2,A项正确;
B. T1℃时,0~100min SiHCl3的转化率为10%,反应的平均速率v(SiHCl3)=![]() =0.0005mol·(L·min)-1,B项错误;
=0.0005mol·(L·min)-1,B项错误;
C. 从图中信息可以看出,T2℃时达到平衡SiHCl3的转化率为20%,则:
2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)
SiH2Cl2(g)+SiCl4(g)
起始量(mol/L) 0.5 0 0
转化量(mol/L) 0.1 0.05 0.05
平衡量(mol/L) 0.4 0.05 0.05,
则平衡常数K=![]() =1/64,C项正确;
=1/64,C项正确;
D. 催化剂不会使平衡移动,不会改变SiHCl3的平衡转化率,D项错误;
答案选AC。

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目