题目内容
【题目】我国科学家研发了一种室温下“可呼吸”的Na-CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:![]() ,下列说法错误的是( )
,下列说法错误的是( )
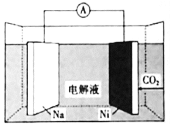
A.放电时,Na为电池的负极
B.充电时释放CO2,放电时吸收CO2
C.放电时,正极反应为:![]()
D.充电时,阳极释放6.72L CO2时,转移的电子数为0.4NA
【答案】D
【解析】
根据电池总反应可知放电时Na被氧化,CO2被还原,所以放电时Na为负极,充电时Na为阴极,放电时Ni为正极吸收CO2,充电时Ni为阳极释放CO2。
A.放电时为原电池,原电池中负极失电子发生氧化反应,根据总反应可知Na被氧化,所以Na为负极,故A正确;
B.根据电池总反应可知,放电时Ni电极吸收二氧化碳发生还原反应为正极,充电时Ni电极发生氧化反应释放二氧化碳,故B正确;
C.根据总反应可知,放电时CO2被还原为正极原料,所以正极反应式为![]() ,故C正确;
,故C正确;
D.未指明温度和压强,无法确定6.72L二氧化碳的物质的量,所以无法确定转移的电子数,故D错误;
故答案为D。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案【题目】通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热(△H)。
化学键 | Cl-Cl | H—H | H—Cl | N≡N |
键能/kJ·mol | 243 | 436 | 431 | 946 |
(1)按要求完成填空
a.2HCl(g) = H2(g)+Cl2(g);△H=______________________
b.N2 (g)+3H2(g)= 2NH3(g) ΔH=-92kJ/mol,则N—H键的键能是__________kJ·mol
(2)1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式__________________________________

(3) 已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2
③ H2O(g) = H2O(l) ΔH3
则CH3OH(l)+O2(g)=CO(g)+ 2H2O(l)ΔH =__________(用含ΔH1、ΔH2、ΔH3的式子表示)
(4)已知:2Al (s)+ 3/2O2(g)==Al2O3(s) △H=-1644.3 kJ mol-1
2Fe (s) +3/2O2(g)==Fe2O3(s) △H=-815.88kJ mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式_______________________。
【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |

(1)该反应的离子方程式 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 < (填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50 mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。(一条即可)
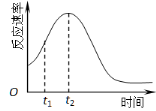 (5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

① ;② 。