题目内容
【题目】下列关于金属腐蚀与防护的说法不正确的是
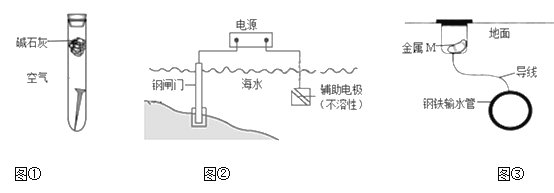
A. 图①,放置于干燥空气中的铁钉不易生锈
B. 图②,若将钢闸门与电源的正极相连,可防止钢闸门腐蚀
C. 图②,若断开电源,钢闸门将发生吸氧腐蚀
D. 图③,若金属M比Fe活泼,可防止输水管腐蚀
【答案】B
【解析】
A.干燥空气中不易形成原电池;
B. 与原电池的正极相连作阳极,易被腐蚀;
C.中性、碱性和弱酸性条件下易发生吸氧腐蚀;
D.M、Fe形成原电池时,Fe作正极。
A.形成原电池需要电解质溶液,所以干燥空气中不易形成原电池,则铁钉不会生锈,所以A选项是正确的;
B. 与原电池的正极相连作阳极,活泼金属作阳极时,金属失电子易被腐蚀,所以若将钢闸门与电源的正极相连,不能防止钢闸门腐蚀,故B错误;
C.中性、碱性和弱酸性条件下易发生吸氧腐蚀,所以钢闸门会发生吸氧腐蚀,所以C选项是正确的;
D. 若金属M比Fe活泼,M、Fe形成原电池时,Fe作正极,M失电子作负极,Fe被保护,所以D选项是正确的。
故答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】铈(Ce)是一种重要的稀土元素。以富含CeO2的废玻璃粉末(含SiO2、 Fe2O3以及其他少量可溶于稀酸的杂质)为原料,采用多种方法回收铈。请回答下列问题:
(1)湿法空气氧化法回收铈的部分流程如下:

已知:CeO2不溶于稀盐酸,也不溶于NaOH溶液。
滤渣的成分是________,反应②的离子方程式是________。
(2)干法空气氧化法回收铈是把Ce(OH)3被空气氧化成Ce(OH)4,氧化过程中发生的化学反应方程式为________。两种制备Ge(OH)4的数据如下表:
干法空气氧化法 | 氧化温度/℃ | 氧化率/% | 氧化时间/h |
暴露空气中 | 110120 | 90 | 18 |
在对流空气氧化炉中 | 110120 | 99 | 8 |
在对流空气氧化炉中大大缩短氧化时间的原因是________。
(3)利用电解方法也可以实现铈的回收。
①在酸性条件下电解Ce2O3 (如图):阳极电极反应式为______,离子交换膜为______ (填“阴”或“阳”)离子交换膜。
②电解产物Ce(SO4)2是重要的氧化剂,将其配成标准溶液,在酸性条件下能测定工业盐中NaNO2的含量,写出发生反应的离子方程式_______。