题目内容
【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |

(1)该反应的离子方程式 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 < (填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50 mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。(一条即可)
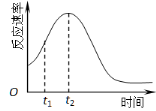 (5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

① ;② 。
【答案】(10分)
(1)2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
(2)浓度;①<②
(3)0.0056
(4)KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间
(5)①该反应放热;②产物Mn2+是反应的催化剂
【解析】
试题分析:(1)酸性KMnO4和H2C2O4反应的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
(2)对比①②实验可探究浓度对化学反应速率的影响,②中A溶液的浓度比①中大,化学反应速率大,所得CO2的体积大,故答案为:浓度;①<②;
(3)CO2的物质的量是:![]() =0.0001mol,设2min末,反应的MnO4-的物质的量为x
=0.0001mol,设2min末,反应的MnO4-的物质的量为x
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
2 10
x 0.0001mol
解得 x=0.00002mol,30×10-3L×0.01mol/L-0.00002mol=0.00028mol,c(MnO4-)=![]() =
=![]() =0.0056mol/L,故答案为:0.0056;
=0.0056mol/L,故答案为:0.0056;
(4)通过测定KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间来比较化学反应速率,故答案为:KMnO4溶液完全褪色所需时间或产生相同体积气体所需的时间;
(5)温度越高,反应速率越快,该反应可能是放热反应;催化剂能加快化学反应的速率,产物Mn2+(或MnSO4)是反应的催化剂,故答案为:①该反应放热;②产物Mn2+是反应的催化剂

 全能练考卷系列答案
全能练考卷系列答案
