��Ŀ����
1���Ȼ���ͭ��CuCl���������л��ϳɹ�ҵ�еĴ�������һ�ְ�ɫ��ĩ������ˮ���������Ҵ���ϡ���ᣮ��ͼ�ǹ�ҵ����ӡˢ��·��ʴ��Һ�ķ�Һ����Fe3+��Cu2+��Fe2+��Cl-������CuCl�����̣�
��Ҫ��ش��������⣺
��1����Һ�ٵ���Ҫ���еĽ�����������Fe2+���ѧ���ţ���ͬ���������ٵ���Ҫ���е�������Fe��Cu��YΪHCl��
��2������Z�����ķ�����ȡ����ʴ��Һ���Թ��У��μ�����Ʒ����Һ����Ʒ����ɫ��֤��Cl2������������ɫ��֤�����㣮
��3��д�����������ɶ�������Ļ�ѧ����ʽCu+2 H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ CuSO4+SO2��+2H2O��
��4��Ϊ�õ�������CuCl���壬��������b������ţ� ����ϴ�ӣ�
a������ˮ b���Ҵ� c��ϡ���� d���Ȼ�ͭ��Һ
��5�����������е�����Һ��pH���ܹ����ԭ���Ƿ�ֹ����������ͭ�������ֹCuClˮ�⣮
��6��д������CuCl�����ӷ���ʽSO2+2Cu2++2Cl-+2H2O�T2CuCl��+SO42-+4H+��
��7���Ȼ���ͭ�Ķ���������
�ٳ�ȡ��Ʒ0.25g����10ml������FeCl3��Һ250ml��ƿ�У�����ҡ�����ڴ���Ʒ�ܽ��ˮ50ml��2��ָʾ������������0.10mol•L-1���������Һ������ɫ����Ϊ�յ㣻���ظ����Σ�������������Һƽ�����Ϊ25.00mL��
��֪��CuCl �ķ���ʽ��Ϊ99��CuCl+FeCl3�TCuCl2+FeCl2��Fe2++Ce4+�TFe3++Ce3+����CuCl�Ĵ���Ϊ99%��
���� Ҫ��������ӡˢ��·�ķ�Һ�Ʊ��Ȼ���ͭ������Ӧ�Ʊ��������ͭ����ҵ��������ӡˢ��·�ķ�Һ����Fe3+��Cu2+��Fe2+��Cl-��������������ۣ����������������۷�Ӧת��Ϊ���������ӣ�ͭ����������Ӧ����ͭ��Ȼ����ˣ�����Ϊ�������������ɵ�ͭ������ͭ���������ԣ��������������ᣬͭ�������Ӧ�����˵õ�������Ϊͭ����Һ���м���Zλ��ˮ������������Ϊ�����ӣ��õ�ʴ��Һ��Ȼ��ͭ��Ũ���ᷴӦ��������ͭ�Ͷ�������ͭ��������Ӧ�����Ȼ�ͭ������ͭ�����������Ȼ�ͭ��Ӧ�����Ȼ���ͭ��
��1��ӡˢ��·�ķ�Һ����Fe3+��Cu2+��Fe2+��Cl-���������������������ܹ�ԭ����Ӧ���ɶ��������ӣ�ͭ�����ܹ�������Ӧ����ͭ�����˺������к���ͭ����������ͭ�����Ļ����ԣ��������������ߣ�
��2������Z�����ķ�����������������Ư���ԣ�����ʹ�л�ɫ�ص�������ɫ��Ƽ��飻
��3�����������ɶ�������ķ�Ӧ��ͭ��Ũ�����ڼ��������·�Ӧ���ɣ�
��4��CuCl��һ�ְ�ɫ��ĩ������ˮ���������Ҵ���ϡ���ᣬ�Ҵ�ϴ�ӿ��Լ���CuCl����ʧ��
��5�����������е�����Һ��pH���ܹ����Ƿ�ֹ��ˮ�����ɳ�����
��6������ͼʾ��֪��CuCl2��CuSO4��SO2��H2O��Ӧ����H2SO4��CuCl�����ݵ�ʧ�����غ���ƽ����ʽ��
��7�����ݷ���ʽ�и���Ӧ����֮��Ĺ�ϵ����CuCl�Ĵ��ȣ�
��� �⣺��ҵ��������ӡˢ��·�ķ�Һ����Fe3+��Cu2+��Fe2+��Cl-��������������ۣ����������������۷�Ӧת��Ϊ���������ӣ�ͭ����������Ӧ����ͭ��Ȼ����ˣ�����Ϊ�������������ɵ�ͭ������ͭ���������ԣ��������������ᣬͭ�������Ӧ�����˵õ�������Ϊͭ����Һ���м���Zλ��ˮ������������Ϊ�����ӣ��õ�ʴ��Һ��Ȼ��ͭ��Ũ���ᷴӦ��������ͭ�Ͷ�������ͭ��������Ӧ�����Ȼ�ͭ������ͭ�����������Ȼ�ͭ��Ӧ�����Ȼ���ͭ��
��1��ӡˢ��·�ķ�Һ����Fe3+��Cu2+��Fe2+��Cl-���������������������ܹ�ԭ����Ӧ���ɶ��������ӣ�ͭ�����ܹ�������Ӧ����ͭ�����˺������к���ͭ�������������ᣬ�������ᷴӦ�����Ȼ�������ͭ�������Ӧ����ͭ���������
�ʴ�Ϊ��Fe2+��Fe��Cu��HCl��
��2��ZΪ����������Z�����ķ�����������������Ư���ԣ�����ʹ�л�ɫ�ص�������ɫ��Ƽ��飬��ȡ����ʴ��Һ���Թ��У��ڵμ�����Ʒ����Һ������Ʒ����ɫ��֤��Cl2������������ɫ��֤�����㣬
�ʴ�Ϊ��ȡ����ʴ��Һ���Թ��У��μ�����Ʒ����Һ����Ʒ����ɫ��֤��Cl2������������ɫ��֤�����㣻
��3�����������ɶ�������ķ�Ӧ��ͭ��Ũ�����ڼ���
�����·�Ӧ���ɣ���Ӧ�Ļ�ѧ����ʽΪ��Cu+2 H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ CuSO4+SO2��+2H2O��
�ʴ�Ϊ��Cu+2 H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ CuSO4+SO2��+2H2O��
��4��������Ϊ�����CuCl��Ʒ�����������ó��˻���ѹ���˷����ٹ��ˣ�������CuCl���岻��ˮ������ˮ�Ҵ�ϴ�ӵ�Ŀ���Ǽ���CuCl����ʧ��
�ʴ�Ϊ��b��
��5�����������е�����Һ��pH���ܹ����ԭ���Ƿ�ֹ����������ͭ�������ֹCuClˮ�⣬
�ʴ�Ϊ����ֹ����������ͭ�������ֹCuClˮ�⣻
��6������ͼʾ��֪��CuCl2��CuSO4��SO2��H2O��Ӧ����H2SO4��CuCl������CuCl�Ļ�ѧ����ʽ���ݵ�ʧ�����غ�õ���CuCl2+CuSO4+SO2+2H2O=2CuCl��+2H2SO4����Ӧ�����ӷ���ʽΪ��SO2+2Cu2++2Cl-+2H2O�T2CuCl��+SO42-+4H+
�ʴ�Ϊ��SO2+2Cu2++2Cl-+2H2O�T2CuCl��+SO42-+4H+��
��7���ζ�0.25g��Ʒ�������������Һ��ƽ�������25.00ml����Ϸ���ʽ��֪��CuCl+FeCl3�TCuCl2+FeCl2��
CuCl�Ĵ���Ϊ$\frac{25.00��1{0}^{-3}L��0.1mol/L��99g/mol}{0.25g}$��100%=99%��
�ʴ�Ϊ��99%��
���� ����Ϊ���������⣬Ϊ�߿��ȵ���ѵ㣬�漰���ʵķ��롢���ʵ��Ʊ�����ȷ���ʵ������ǽ���ؼ���ע���������ʵ�����Ӧ�ã���Ŀ�ѶȽϴ�

 ��У����ϵ�д�
��У����ϵ�д�| A�� | �����������γ�ˮ����ζ����Ҫ�ɷ� | |
| B�� | ��֬��������Ӧ����֬����ͱ��� | |
| C�� | �����ʵ�ˮ����ﶼ����ȩ���Ͱ��� | |
| D�� | ������ﶼ������ͬ�Ĺ����� |
| A�� | 2H2��g��+O2��g��=2H2O��g����H1�� 2H2��g��+O2��g��=2H2O��l����H2 | |
| B�� | S��g��+O2��g��=SO2��g����H1�� S��s��+O2��g��=SO2��g����H2 | |
| C�� | $\frac{1}{2}$C��s��+O2��g��=CO��g����H1�� C��s��+O2��g��=CO2��g����H2 | |
| D�� | HCl��g��=$\frac{1}{2}$H2��g��+$\frac{1}{2}$Cl2��g����H1�� H2��g��+Cl2��g��=2HCl��g����H2 |
| A�� |  ��ȥCO��CO2 | B�� |  ��ȡʱ���Һ | ||
| C�� | 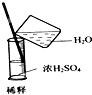 ϡ��Ũ���� | D�� |  ���Թ��еμ�Һ�� |
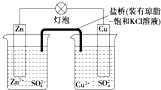
| A�� | ������ӦΪ��Zn-2e-�TZn2+ | B�� | �����е�K+����ZnSO4��Һ | ||
| C�� | �����·�У������Ӹ����������� | D�� | ��ط�ӦΪ��Zn+Cu2+�TZn2++Cu |
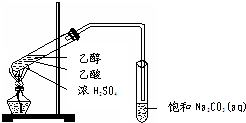 ʵ��������ͼ��ʾ��װ����ȡ����������
ʵ��������ͼ��ʾ��װ����ȡ���������� CH3COOC2H5+H2O�������������ܶȱ�ˮС�����С�������з���ζ��
CH3COOC2H5+H2O�������������ܶȱ�ˮС�����С�������з���ζ�� �Ĵ�����屶�ӣ����屶��Ϊԭ�Ͽ��Ƶû�����A��A�Ľṹ��ʽ��ͼ��ʾ��
�Ĵ�����屶�ӣ����屶��Ϊԭ�Ͽ��Ƶû�����A��A�Ľṹ��ʽ��ͼ��ʾ��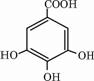 ��
��