题目内容
12.在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )| A. | 2H2(g)+O2(g)=2H2O(g)△H1; 2H2(g)+O2(g)=2H2O(l)△H2 | |
| B. | S(g)+O2(g)=SO2(g)△H1; S(s)+O2(g)=SO2(g)△H2 | |
| C. | $\frac{1}{2}$C(s)+O2(g)=CO(g)△H1; C(s)+O2(g)=CO2(g)△H2 | |
| D. | HCl(g)=$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)△H1; H2(g)+Cl2(g)=2HCl(g)△H2 |
分析 A、液态水变为气态水的过程是吸热过程;
B、固体硫变为气态硫需要吸收热量;
C、碳单质完全燃烧放热多于不完全燃烧放的热;
D、H2(g)+Cl2(g)=2HCl(g)该反应是放热反应,焓变是负值;其逆反应是吸热反应,焓变是正值.
解答 解:A、物质的燃烧反应是放热的,所以焓变是负值,液态水变为气态水的过程是吸热的,故△H1>△H2,故A错误;
B、物质的燃烧反应是放热的,所以焓变是负值,固体硫变为气态硫需要吸收热量,所以△H1<△H2,故B正确;
C、碳单质完全燃烧生成二氧化碳放热多于不完全燃烧生成一氧化碳放的热,反应的焓变是负值,故△H1>△H2,故C错误;
D、H2(g)+Cl2(g)=2HCl(g)该反应是放热反应,焓变是负值;其逆反应是吸热反应,焓变是正值,所以△H1>△H2,故D错误;
故选B.
点评 本题考查了物质反应能量变化分析判断,主要是盖斯定律的应用,物质量不同、状态不同、产物不同,题目较简单.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
2.海洋约占地球表面的71%,具有十分巨大的开发潜力,目前的南海争端威胁到我们国家的核心利益.通过海水资源的开发利用不能得到的是( )
| A. | 石油、天然气 | B. | 铀和重水 | C. | 淡水 | D. | 钠、钾、镁、溴 |
20.下列说法正确的是( )
| A. | 环保热词“PM2.5”是指大气中直径小于或等于2.5 微米(1微米=1×10-6米)的颗粒,“PM2.5”与空气形成的分散系属于胶体 | |
| B. | 食盐中加入少量碘化钾,食用后可补充人体内碘元素的不足 | |
| C. | 石油催化裂化的主要目的是提高汽油等轻质油的产量与质量,石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃 | |
| D. | 晶体硅是通信工程中制作光导纤维的主要原料 |
17.对实验过程中出现的异常现象进行探究,是实施素质教育、培养创新精神的有效途经.
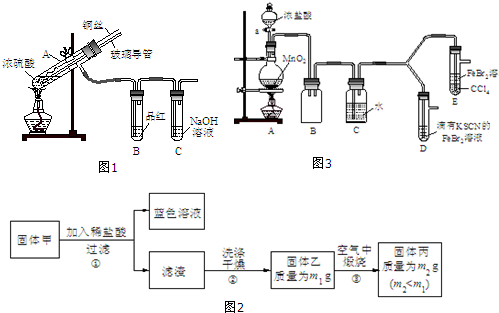
【实验1】用图1实验装置进行铜与浓硫酸的反应,实验中发现试管内除了产生白色硫酸铜固体外,在
铜丝表面还有黑色固体甲生成,甲中可能含有黑色的CuO、CuS、Cu2S.查阅资料:CuS和Cu2S均为黑色固体,常温下都不溶于稀盐酸,在空气中煅烧,均转化为CuO和SO2.为了探究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图2实验:
(1)上述实验装置除了有尾气吸收装置外,还有一个显著的优点是在熄灭酒精灯后,B中的液体不会倒吸.
(2)固体乙在空气中煅烧时,使用的实验仪器除了玻璃棒、三脚架、酒精灯外,还必须有泥三角、坩埚(坩埚钳).
(3)确定乙是否煅烧完全的操作是重复操作(再煅烧、冷却、称量),直至恒重(前后两次称量差不超过0.001g).
(4)煅烧过程中一定发生的化学反应方程式为2CuS+3O2$\frac{\underline{\;煅烧\;}}{\;}$2CuO+2SO2.
【实验2】某化学兴趣小组设计了如图3实验装置(尾气吸收装置未画出),探究Cl2、Br2、Fe3+的氧化性强弱.
(5)根据下列实验操作和现象,填写实验结论.
(6)因忙于观察和记录,没有及时停止反应,D、E中均发生了异常的变化:D装置中,红色慢慢褪去;E装置中,CCl4层先由无色变为橙色,后颜色逐渐加深,直至变成红色.
为探究上述实验现象的本质,小组同学查得资料如下:
①请用平衡移动原理(结合化学用语)解释Cl2过量时D中溶液红色褪去的原因过量氯气和SCN-反应:2SCN-+Cl2=2Cl-+(SCN)2,使SCN-浓度减小,则Fe3++3SCN-?Fe(SCN)3平衡逆向移动而褪色;
请设计简单实验证明上述解释取少量褪色后的溶液,滴加KSCN溶液,若溶液变红色,则上述推测合理,或取少量褪色后的溶液,滴加FeCl3溶液,若溶液不变红,则上述推测合理.
②欲探究E中颜色变化的原因,设计实验如下:用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生.请结合化学用语解释仅产生白色沉淀的原因BrCl+H2O=HBrO+HCl反应只产生Cl-,不产生Br-.

【实验1】用图1实验装置进行铜与浓硫酸的反应,实验中发现试管内除了产生白色硫酸铜固体外,在
铜丝表面还有黑色固体甲生成,甲中可能含有黑色的CuO、CuS、Cu2S.查阅资料:CuS和Cu2S均为黑色固体,常温下都不溶于稀盐酸,在空气中煅烧,均转化为CuO和SO2.为了探究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图2实验:
(1)上述实验装置除了有尾气吸收装置外,还有一个显著的优点是在熄灭酒精灯后,B中的液体不会倒吸.
(2)固体乙在空气中煅烧时,使用的实验仪器除了玻璃棒、三脚架、酒精灯外,还必须有泥三角、坩埚(坩埚钳).
(3)确定乙是否煅烧完全的操作是重复操作(再煅烧、冷却、称量),直至恒重(前后两次称量差不超过0.001g).
(4)煅烧过程中一定发生的化学反应方程式为2CuS+3O2$\frac{\underline{\;煅烧\;}}{\;}$2CuO+2SO2.
【实验2】某化学兴趣小组设计了如图3实验装置(尾气吸收装置未画出),探究Cl2、Br2、Fe3+的氧化性强弱.
(5)根据下列实验操作和现象,填写实验结论.
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯. | D装置中:溶液变红 E装置中:水层溶液变黄,振荡后,CCl4层无明显变化. | Cl2、Br2、Fe3+的氧化性由强到弱的顺序为: Cl2>Br2>Fe3+ |
为探究上述实验现象的本质,小组同学查得资料如下:
| ⅰ.(SCN)2性质与卤素单质类似.氧化性:Cl2>(SCN)2. ⅱ.Cl2和Br2反应生成的BrCl呈红色,沸点约5℃,与水发生水解反应. ⅲ.AgClO、AgBrO均可溶于水. |
请设计简单实验证明上述解释取少量褪色后的溶液,滴加KSCN溶液,若溶液变红色,则上述推测合理,或取少量褪色后的溶液,滴加FeCl3溶液,若溶液不变红,则上述推测合理.
②欲探究E中颜色变化的原因,设计实验如下:用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生.请结合化学用语解释仅产生白色沉淀的原因BrCl+H2O=HBrO+HCl反应只产生Cl-,不产生Br-.
4.下列Ⅰ、Ⅱ叙述正确并且有因果关系的是( )
| 选项 | Ⅰ | Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | Fe3+有氧化性 | 利用30%的FeCl3溶液腐蚀铜箔制造印刷线路板 |
| D | C12有剧毒 | 大量氯气泄漏时,用烧碱溶液浸湿软布蒙面,并迅速离开现场 |
| A. | A | B. | B | C. | C | D. | D |
3.下列说法不正确的是( )
| A. | 通常状况下,金属钠中的金属键比金属钾中的金属键强 | |
| B. | 晶格能的大小反映了离子晶体开始分解温度的高低 | |
| C. | 离子键没有方向性和饱和性 | |
| D. | 在晶胞中处于立方体顶点的一种或离子为8个晶胞共享 |
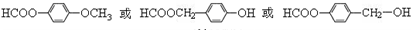 .
.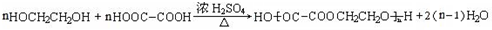 .
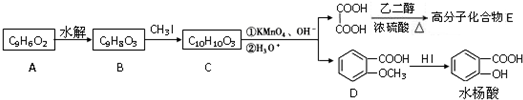
.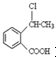 为原料制备
为原料制备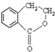 的合成路线流程图(无机试剂任用),并注明反应条件.合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$
的合成路线流程图(无机试剂任用),并注明反应条件.合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$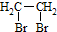 .
.
 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;