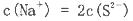下列物质的水溶液经加热浓缩,蒸干灼烧仍能得到原物质的是( )
| A.FeC13 | B.Ca(HCO3)2 | C.Na[Al (OH)4] | D.Na2SO3 |
下列关于盐类水解原理的叙述正确的是( )
| A.一定生成弱酸 | B.水的电离平衡不受影响 |
| C.水解过程中要吸收热量 | D.溶液的pH一定变大 |
下列说法正确的是
| A.强电解质的水溶液中不存在溶质分子,弱电解质的水溶液中存在溶质分子和离子 |
| B.强电解质的水溶液导电性强于弱电解质的水溶液 |
| C.强电解质都是离子化合物,弱电解质都是共价化合物 |
| D.强电解质易溶于水,弱电解质难溶于水 |
已知温度T时水的离子积常数为 。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
| A.a=b |
| B.混合溶液的pH=7 |
C.混合溶液中, |
D.混合溶液中, |
下列叙述正确的是
| A.c(H+)等于l×l0-7mol/L的溶液一定是中性溶液 |
| B.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其Kw= l×l0-14 |
| C.将水加热,Kw增大,pH不变 |
| D.任何浓度的溶液都可以用pH来表示其酸性的强弱 |
已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和CrO42-,浓度均为0.010mol?L-1,向该溶液中逐滴加入0.010 mol?L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
| A.Cl-、Br-、CrO42- | B.CrO42-、Br-、Cl- | C.Br-、Cl-、CrO42- | D.Br-、CrO42-、Cl- |
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
| A.pH=4的醋酸中:c(H+)=4.0molL-1 |
| B.饱和小苏打溶液中:c(Na+)= c(HCO3-) |
| C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol?L-1 |

 NaOH溶液中逐滴加入。0.2mol
NaOH溶液中逐滴加入。0.2mol