题目内容
下列说法正确的是:
A相同温度时,1mol/L氨水与05mol/L氨水中,c(OH-)之比是2:1
B.1mol/L氯化铵 溶液中c(NH4+)=c(Cl-)
C.0.1mol/LCH3COONa溶液中加少量CH3COOH溶液,使溶液呈中性,此时混合液中
D.硫化钠溶液中,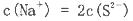
C
解析试题分析:A、氨水为弱电解质,不能完全电离,故A 错误;B、铵根离子水解使溶液显酸性,导致铵根离子浓度小于氯离子,B错误;C、根据电荷守恒知c(Na+)+c(H+)=c(CH3COO-)+c(OH-),溶液呈中性说明c(H+)=c(OH-),c(Na+)=c(CH3COO-),正确;D、硫离子在溶液中会发生水解,故D错误。
考点:考查弱电解质的电离、盐类水解及溶液中离子浓度关系等相关知识。

练习册系列答案
相关题目
下列物质的水溶液中,呈碱性的是
| A.Na2CO3 | B.Na2SO4 | C.NH4Cl | D.KAl (SO4) 2 |
将pH=5的H2SO4溶液稀释1000倍后,溶液中SO42-离子浓度与H+离子浓度的比值约为( )
| A.1:10 | B.1:1 | C.1:2 | D.1:20 |
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
| A.pH=4的醋酸中:c(H+)=4.0molL-1 |
| B.饱和小苏打溶液中:c(Na+)= c(HCO3-) |
| C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol?L-1 |
在Na2S溶液中下列关系不正确的是( )
| A.c(Na+)=2c(HS-)+c(S2-)+c(H2S) |
| B.c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) |
| C.c(Na+)> c(S2-)>c(OH-)>c(HS-) |
| D.c(OH-)=c(HS-)+c(H+)+2c(H2S) |
已知下列弱酸的电离常数:
H2CO3: Ka1=4.30×10-7 ;Ka2=5.61×10-11
H2SO3: Ka1=1.54×10-2;Ka2=1.02×10-7
HClO:Ka=2.95×10-8
下列离子在溶液中结合H+的能力不正确的是
A.HCO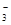 >HSO3- >HSO3- | B.CO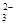 >SO >SO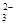 | C.HCO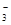 >ClO- >ClO- | D.ClO->SO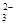 |
下列说法正确的是( )
| A.在氨水中加入少量的水或氯化铵固体后,都能使溶液中的c(OH-)减小 |
| B.反应Hg(l)+H2SO4(aq)===HgSO4(aq)+H2(g)在常温下不能自发进行,则ΔH<0 |
| C.工业电解食盐水中,电解池被阳离子交换膜隔成阴极室和阳极室,目的是避免阳极产生的气体与烧碱反应 |
| D.在等浓度的NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl沉淀,则Ksp(AgCl)<Ksp(Ag2CrO4) |
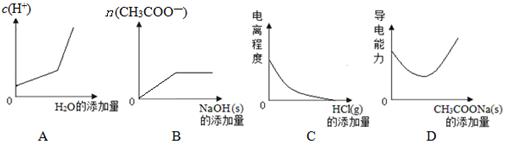
 H+ + A2- (Ka=1.0×10-2),下列说法正确的是
H+ + A2- (Ka=1.0×10-2),下列说法正确的是