将Mg、Cu组成的混合物26.4g投入到适量的稀硝酸中,固体完全溶解,收集到标准状况下的NO气体8.96L,向反应后的溶液中加入过量的5mol·L-1的NaOH溶液300mL,金属离子完全沉淀。则形成沉淀的质量是 ( )
| A.43.2g | B.46.8g | C.53.6g | D.63.8g |
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下气体的体积为(设反应中HNO3被还原成NO)( )
| A.0.448L | B.0.672L | C.0.896L | D.0.224L |
若NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
| A.16g CH4与18 g NH4+所含质子数相等 |
| B.1mol 苯分子中含有碳碳双键数为3NA |
| C.将分子总数为NA的NH3和HCl的混合气体置于标准状况下,其体积为约22. 4L |
| D.7.8 g Na2O2中含有的离子总数目为0.3NA |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.在反应KIO3 + 6 HI=KI + 3I2+3 H2O中,每生成3mo1 I2转移的电子数为5NA |
| B.100mL 18.4mo1·L-1硫酸与足量Cu反应,生成SO2的分子数为0.92NA |
| C.1L 0.1 moI·L-1的CH3COOH溶液中所含的离子和分子总数为0.1NA |
| D.将0.lmol FeC13滴人沸水中可制得0.1NA Fe(OH)3胶粒 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.等物质的量的N2和CO所含分子数均为NA |
| B.标准状况下,11.2 L氟化氢所含的分子数为0.5NA |
| C.常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.5NA |
| D.常温常压下,14.9g KCl与NaClO的混合物中含氯元素的质量为7.1g |
单质碳和氧化铜在一定温度下反应时,氧化铜可被还原为Cu2O、Cu。现将2.00g C与16.0g CuO的混合物,隔绝空气加热一段时间后,将生成的气体通过足量的澄淸石灰水,共收集到1.12 L气体(标准状况),生成沉淀的质量为5.00 g。下列说法错误的是
| A.反应后的固体混合物中还含有碳 |
| B.反应后的固体混合物中Cu的质量为12.8 g |
| C.反应后的固体混合物总质貴为14.4 g |
| D.反应后的固体混合物中氧化物的物质的量为0.05mol |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.0.1 mol Fe在0.1mol CL2中充分燃烧,转移的电子数为0.3NA |
| B.标准状况下,11.2 L CCl4所含分子数约为0.5NA |
| C.常温下,pH=13的NaOH溶液中,OH-的数目为0.1NA |
| D.常温、常压下,14g CO与N2的混合气含的原子数为NA |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.24g NaH中阴离子所含电子总数为NA |
| B.标准状况下,22.4 L苯中含有C—H键数目为6NA |
| C.在碳酸钠溶液中,若c(CO32-)="1" mol?L-1,则c(Na+)="2" mol?L-1 |
| D.通过MnO2催化使H2O2分解,产生32gO2时转移电子数为2NA |
下列表示方法正确的是( )
A.铜的原子结构示意图: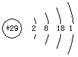 |
| B.S2- 核外电子排布式:[Ne] 2s23p6 |
C.O原子处于基态的轨道表示式: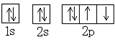 |
D.用电子式表示MgCl2的形成:Mg:+ → →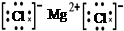 |