题目内容
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
①常温常压下,17 g重甲基(-14CD3)所含的中子数为11NA;
②常温常压下,22.4 L NO气体的分子数小于NA;
③64 g铜发生氧化还原反应,一定失去2NA个电子;
④室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA;
⑤1 mol铁铝混合物与足量稀盐酸反应时,转移电子数是3 NA;
⑥常温常压下,1 mol氦气含有的核外电子数为4NA;
⑦6.8g熔融的KHSO4中含有的阳离子数为0.05 NA;
| A.①② | B.③④⑦ | C.②④⑦ | D.②⑤⑥ |
C
解析试题分析:①-14CD3的中子数为11,17g含17g÷20g/mol×11<11mol,错;
②常温为25℃,高于标准状况温度,摩尔体积>22.4mol?L?1,所以正确;
③铜与硫反应,铜失1个电子,64 g铜发生氧化还原反应,有可能失去NA个电子;
④乙烯和丁烯的最简式相同,含C原子的物质的量为:21.0g÷14g/mol=1.5mol;
⑤铁原子失去2个电子,所以⑤错误;
⑥氦为单原子分子,1 mol氦气含有的核外电子数为2NA;
⑦熔融的KHSO4中含有的阳离子为K+,则6.8g熔融的KHSO4中含阳离子:
6.8g÷136g/mol=0.05mol。
考点:本题考察阿伏伽德罗常数及其综合应用。

下列对有关化学用语的理解错误的是
A.电子式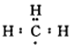 可以表示甲基,但是不可以表示CH+3 可以表示甲基,但是不可以表示CH+3 |
B.离子结构示意图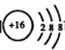 可以表示 可以表示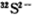 ,又可以表示34S2— ,又可以表示34S2— |
C.比例模型: 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 |
| D.分子式C3H3O既可以表示1-丙醇,也可以表示2-丙醇 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
| A.25℃时,pH=1的1.0 LH2SO4溶液中含有的H+的数目为0.2NA |
| B.标准状况下,2.24 LCl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
| C.室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D.取0.5 L 0.2 mol·L-1mol氯化铁溶液 ,所得溶液含有0.1 NA个Fe3+ |
将15.2gFe、Cu组成的合金溶于过量的稀硝酸中,生成4.48LNO(标准状况),向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量为
| A.33.2g | B.25.4g | C.22.4g | D.19.6g |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.24g NaH中阴离子所含电子总数为NA |
| B.标准状况下,22.4 L苯中含有C—H键数目为6NA |
| C.在碳酸钠溶液中,若c(CO32-)="1" mol?L-1,则c(Na+)="2" mol?L-1 |
| D.通过MnO2催化使H2O2分解,产生32gO2时转移电子数为2NA |
对相同状况下的12C18O和14N2两种气体,下列说法正确的是
| A.若质量相等,则质子数相等 |
| B.若原子数相等,则中子数相等 |
| C.若分子数相等,则体积相等 |
| D.若体积相等,则密度相等 |
设阿伏加德罗常数的值为NA,下列说法正确的是
| A.在常温常压下,11.2LN2含有的分子数为0.5NA |
| B.在常温常压下,1molH2含有的原子数为2NA |
| C.0.1mol/LNaCl溶液中含有Na+数目为0.1NA |
| D.在同温同压时,相同体积的任何气体含有相同数目的原子 |
以下化学用语正确的是
| A.苯的实验式: C6H6 | B.乙醇的分子式: CH3CH2OH |
| C.乙烯的结构简式: CH2CH2 | D.甲醛的结构式: |
下列微粒中,对水的电离平衡不产生影响的是
A. | B.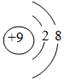 | C.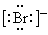 | D.1s22s22p63s1 |