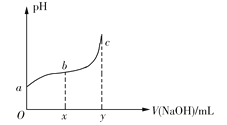
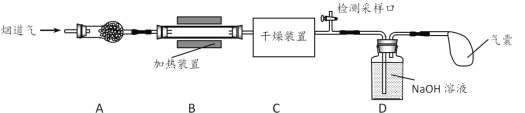
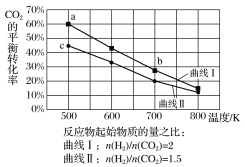
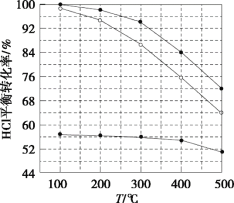
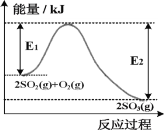
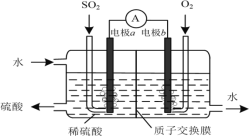
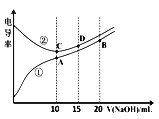
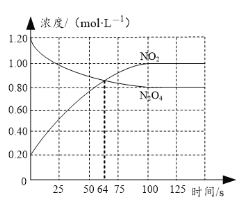
0 197016 197024 197030 197034 197040 197042 197046 197052 197054 197060 197066 197070 197072 197076 197082 197084 197090 197094 197096 197100 197102 197106 197108 197110 197111 197112 197114 197115 197116 197118 197120 197124 197126 197130 197132 197136 197142 197144 197150 197154 197156 197160 197166 197172 197174 197180 197184 197186 197192 197196 197202 197210 203614