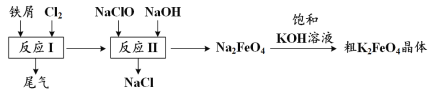题目内容
【题目】一定条件下,反应:6H2(g)+2CO2(g)![]() C2H5OH(g)+3H2O(g)的数据如图所示。
C2H5OH(g)+3H2O(g)的数据如图所示。
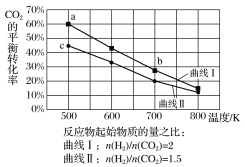
下列说法正确的是( )
A.该反应为吸热反应
B.达平衡时,v正(H2)=v逆(CO2)
C.b点对应的平衡常数K值大于c点
D.a点对应的H2的平衡转化率为90%
【答案】D
【解析】
A. 由图象可知,升高温度,CO2的平衡转化率降低,平衡逆向移动,所以该反应为放热反应,故A错误;
B. 达平衡时,正逆反应速率比等于系数比,即 v正(H2)=3v逆(CO2),故B错误;
C. 正反应放热,升高温度,平衡常数减小,b点对应的平衡常数K值小于c点,故C错误;
D.曲线Ⅰ H2、CO2的投料比为2:1,设投入H2、CO2的物质的量分别是2mol、1mol,a点CO2的平衡转化率为60%,则消耗CO2 0.6mol、消耗H2 1.8mol,所以a点对应的H2的平衡转化率为![]() 90%,故D正确;
90%,故D正确;
选D。

 优加精卷系列答案
优加精卷系列答案【题目】元素周期表与元素周期律在学习、研究中有很重要的作用。下表是元素周期表中6种元素的相关信息,其中Q、W、X位于同一周期。
元素 | 信息 |
Q | 单质是稳定的半导体材料,用于制造芯片 |
W | 最高化合价为+7价 |
X | 最高价氧化物对应的水化物在本周期中碱性最强 |
Y | 焰色反应为紫色(透过蓝色钴玻璃片) |
Z | 地壳中含量最高的金属元素,其合金可用于制造飞机外壳 |
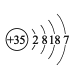
M | 原子结构示意图为 |
(1)Q元素所在周期表的位置为_____。
(2)W单质的电子式为_____。
(3)Z的单质与X的最高价氧化物对应的水化物反应的离子方程式为_____。
(4)Y的金属性强于X,请结合原子结构解释其原因_____。
(5)下列对于M及其化合物的推断中,正确的是_____(填序号)。
①M的最低负化合价与W的最低负化合价相同
②M的氢化物的稳定性弱于W的氢化物的稳定性
③M的单质可与X和W形成的化合物的水溶液发生置换反应
(6)与M位于同一主族,电子层数比M多一层的元素在生活中的用途是_____(写出一条即可)。