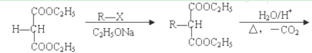
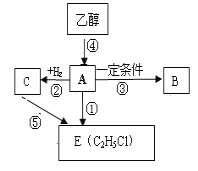
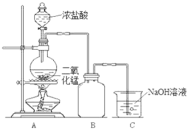
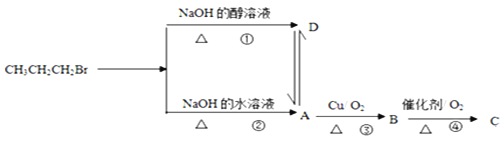
0 196699 196707 196713 196717 196723 196725 196729 196735 196737 196743 196749 196753 196755 196759 196765 196767 196773 196777 196779 196783 196785 196789 196791 196793 196794 196795 196797 196798 196799 196801 196803 196807 196809 196813 196815 196819 196825 196827 196833 196837 196839 196843 196849 196855 196857 196863 196867 196869 196875 196879 196885 196893 203614