18.下列混合物的分离或提纯方法不正确的是( )
| A. | 用分液漏斗分离溴乙烷和水的混合物 | |
| B. | 用结晶的方法分离氯化钠和硝酸钾的混合物 | |
| C. | 除去含有少量硝酸钡杂质的硝酸钾,可以加入过量的碳酸钾溶液,过滤后除去沉淀,在滤液中加入适量硝酸调至溶液的pH为7 | |
| D. | 除去乙酸乙酯中的少量乙酸,可以加入乙醇和浓硫酸加热,使乙酸全部转化为乙酸乙酯 |
16.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1:1 | |
| B. | 常温下,0.1 mol•L-1 NH4NO3溶液中含有的氮原子数是0.2NA | |
| C. | 常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA | |
| D. | 1mol 甲基所含电子数约为10NA |
15.氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是( )
| A. | AlON和石英的化学键类型相同 | |
| B. | AlON和石英晶体类型相同 | |
| C. | AlON中N元素的化合价为-1 | |
| D. | 电解熔融AlON或电解熔融Al2O3都能得到Al |
12.现有常温下pH=2的盐酸甲和pH=2的醋酸溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)>pH(乙)( 填“>”、“<”或“=”).
(3)已知25℃时,酸的电离平衡常数如下:
写出下列反应的离子方程式:
CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;
HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)>pH(乙)( 填“>”、“<”或“=”).
(3)已知25℃时,酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | -- | 5.6×10-11 | -- |
CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;
HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
9.实验中发生下列事故,处理方法正确的是( )
0 173462 173470 173476 173480 173486 173488 173492 173498 173500 173506 173512 173516 173518 173522 173528 173530 173536 173540 173542 173546 173548 173552 173554 173556 173557 173558 173560 173561 173562 173564 173566 173570 173572 173576 173578 173582 173588 173590 173596 173600 173602 173606 173612 173618 173620 173626 173630 173632 173638 173642 173648 173656 203614
| A. | 钠着火用泡沫火器扑灭 | |
| B. | 苯酚沾在手上,应马上用NaOH溶液洗 | |
| C. | 皮肤上沾有浓硫酸,立即用量水冲洗 | |
| D. | 酒精灯在桌上歪倒失火后,立即用湿布盖上 |

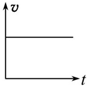

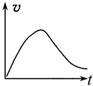
 ;B的结构简式是
;B的结构简式是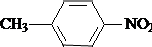 .
. 用二氧化氯(ClO2)、高铁酸钠(Na2FeO4摩尔质量为166g•mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.
用二氧化氯(ClO2)、高铁酸钠(Na2FeO4摩尔质量为166g•mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.