题目内容
15.氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是( )| A. | AlON和石英的化学键类型相同 | |
| B. | AlON和石英晶体类型相同 | |
| C. | AlON中N元素的化合价为-1 | |
| D. | 电解熔融AlON或电解熔融Al2O3都能得到Al |
分析 氮氧化铝(AlON)属原子晶体,石英(SiO2)属于原子晶体,原子晶体中只含有共价键,熔融时不导电,Al2O3属于离子晶体,结合选项来解答.
解答 解:A.AlON和石英均属于原子晶体,均只含有共价键,故A正确;
B.AlON和石英均属于原子晶体,故B正确;
C.AlON中O为-2价,Al为+3价,所以N元素的化合价为-1,故C正确;
D.AlON属于原子晶体只含有共价键熔融时不导电,而Al2O3属于离子晶体,熔融时能导电,所以电解熔融Al2O3能得到Al,故D错误;
故选D.
点评 本题考查化学键和晶体类型,明确信息及常见物质的晶体类型、含有的化学键即可解答,题目难度不大,注意原子晶体只含有共价键熔融时不导电.

练习册系列答案
相关题目
6.运输浓硫酸的车辆上贴有的危险化学品标志是( )
| A. |  | B. |  | C. |  | D. |  |
3.下列说法正确的是( )
| A. | 制氧气时,用Na2O2或H2O2作反应物应该选择不同的气体发生装置 | |
| B. | 某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- | |
| C. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀时的离子方程式为:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
7.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答下列问题:
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱若a=7,HA为强酸;若a>7,HA为弱酸.
(2)不考虑其它组的实验结果,单从乙组情况分析,c1是否一定等于0.2mol/L否(填“是”或“否”).混合溶液中离子浓度c(A-)与c(Na+)的大小关系是C.
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是弱酸(填“强”或“弱”).该混合溶液中c(A-)+c(HA)=c(Na+)或0.05mol/L.
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c1 | 0.2 | pH=7 |
| 丙 | 0.1 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱若a=7,HA为强酸;若a>7,HA为弱酸.
(2)不考虑其它组的实验结果,单从乙组情况分析,c1是否一定等于0.2mol/L否(填“是”或“否”).混合溶液中离子浓度c(A-)与c(Na+)的大小关系是C.
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是弱酸(填“强”或“弱”).该混合溶液中c(A-)+c(HA)=c(Na+)或0.05mol/L.
4.下列应用不涉及氧化还原反应的是( )
| A. | Na2O2用作呼吸面具的供氧剂 | B. | 工业上电解熔融状态Al2O3制备Al | ||
| C. | 工业上利用合成氨实现人工固氮 | D. | 实验室用NH4Cl 和Ca(OH)2制备NH3 |
5.人工光合系统装置(如图)可实现以CO2和H2O合成CH4.下列有关说法不正确的是( )

| A. | 该装置为原电池,且铜为正极 | |
| B. | 电池工作时,H+向Cu电极移动 | |
| C. | GaN电极表面的电极反应式为:2H2O-4e-═O2+4H+ | |
| D. | 反应CO2+2H2O═CH4+2O2中每消耗1mol CO2转移4mol e- |
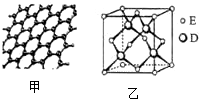 原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题: