题目内容
17.将锌粒投入一定浓度的稀硫酸中,实际反应速率和时间的关系与下图最接近的是( )| A. |  | B. | 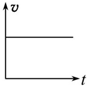 | C. |  | D. | 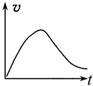 |
分析 锌与硫酸的浓度为放热反应,反应开始后温度升高,速率增大,但随着反应的进行,溶液浓度逐渐减小,结合浓度对反应速率的影响解答.
解答 解:锌与硫酸的浓度为放热反应,反应开始后温度升高,速率增大,但随着反应的进行,溶液浓度逐渐减小,则速率逐渐减小,应为 ,
,
故选D.
点评 本题考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大,注意把握影响化学反应速率的因素与影响原因的关系.

练习册系列答案
相关题目
7.下列实验操作或结论正确的是( )
| A. | 鉴别乙烷与乙烯或除去乙烷中的少量乙烯杂质都可用高锰酸钾酸性溶液 | |
| B. | 某同学需用480 mL 2.0 moI•L-1氢氧化钠溶液进行实验,则配制该溶液时他称取氢氧化钠固体质量一定是38.4 g | |
| C. | 向含Fe3+的溶液中加入KSCN溶液时一定有红褐色沉淀产生 | |
| D. | 硝酸钾和稀硫酸的混合溶液中加入铜粉后,溶液会慢慢变蓝 |
5.在密闭容器中,加热2amol的NaHCO3和amol的Na2O2的固体混合物,充分反应后,容器中的固体剩余物是( )
| A. | Na2CO3和NaOH | B. | Na2CO3 | ||
| C. | NaOH和Na2O2 | D. | NaOH、Na2O2和Na2CO3 |
12.现有常温下pH=2的盐酸甲和pH=2的醋酸溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)>pH(乙)( 填“>”、“<”或“=”).
(3)已知25℃时,酸的电离平衡常数如下:
写出下列反应的离子方程式:
CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;
HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍.稀释后的溶液,其pH大小关系为:pH(甲)>pH(乙)( 填“>”、“<”或“=”).
(3)已知25℃时,酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | -- | 5.6×10-11 | -- |
CH3COOH+Na2CO3(少量):2CH3COOH+CO32-=H2O+2CH3COO-+CO2↑;
HClO+Na2CO3(少量):HClO+CO32-=ClO-+HCO3-.
2.化学与人类生产、生活密切相关,下列说法正确的是( )
| A. | 铁的冶炼过程是通过置换反应得到单质铁 | |
| B. | 太阳能电池可采用硅材料制作,其应用有利于环保、节能 | |
| C. | 化学家采用玛瑙研钵磨擦固体反应物进行溶剂合成,玛瑙的主要成分是硅酸盐 | |
| D. | 包装食品里常有硅胶、生石灰、还原铁粉三类小包,其作用相同 |
7.下列设计的实验方案能达到实验目的是( )
| A. | 通过灼热的镁粉除去N2中的O2 | |
| B. | 用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2 | |
| C. | 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体 | |
| D. | 检验溶液中是否有SO42-:先将溶液用足量的盐酸酸化,再加入BaCl2溶液 |