10.完全沉淀等体积、等物质的量浓度的AgNO3溶液,需要加入等浓度的NaCl、MgCl2、AlCl3溶液的体积之比为( )
| A. | 1:1:1 | B. | 3:2:1 | C. | 6:3:2 | D. | 1:2:3 |
9.下列对某些离子的检验实验,现象及结论一定正确的是( )
| 选项 | 实验方法 | 现象 | 结论 |
| 向某溶液加入AgNO3溶液 | 出现白色沉淀 | 原溶液中一定有Cl- | |
| 向某溶液加入BaCl2溶液 | 出现白色沉淀 | 原溶液中一定有SO42- | |
| 向某溶液加入NaOH溶液 | 出现蓝色沉淀 | 原溶液中一定有Cu2+ | |
| 向某溶液加入H2SO4溶液 | 产生无色无味气体 | 原溶液中一定有CO32- |
| A. | A | B. | B | C. | C | D. | D |
8.下列溶液中溶质的物质的量浓度为1mol/L的是( )
| A. | 将40g NaOH固体溶解于1L水中 | |
| B. | 将22.4L氯化氢气体溶于水配成lL溶液 | |
| C. | 将1L 10mol/L的浓盐酸与9L水混合 | |
| D. | 20g NaOH固体溶解在水中配成500mL溶液 |
7. 资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.
资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.
(1)兴趣小组同学认为,上述反应的生成物可能与反应温度(T),KOH溶液的浓度(C)有关.他们做了如下对比实验(每次反应中硫粉的质量、KOH溶液的体积均相同).
实验①~④是探究温度对生成物的影响,⑤~⑧是探究KOH溶液的浓度对生成物的影响.请在表中相应空格填入相应数据.
(2)兴趣小组设计实验对上述反应中生成的盐的成分进行探究.他们提出如下假设,请你根据氧化还原反应的规律,完成假设二和假设三:
假设一:生成的盐是K2S和K2SO3;
假设二:生成的盐是K2S和K2SO4;
假设三:生成的盐是K2S,K2SO3和K2SO4;
(3)请你设计实验验证上述假设一.完成下表中内容.(除了硫粉与热的KOH溶液的反应液之外,可供选择的药品有稀硝酸,稀盐酸等;已知:6H++SO32-+2S2-=3S+3H2O)
(4)兴趣小组通过改变硫粉的质量,得出生成钾盐的质量与硫粉质量的变化关系如图所示.有人据此得出结论:生成的盐一定是K2S和K2SO3的混合物.请你根据计算结果指出该结论是否正确:不正确.
(5)请分析上述反应中有K2SO4生成的可能原因是:亚硫酸钾具有还原性,很容易被氧气氧化为硫酸钾.
 资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.
资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.(1)兴趣小组同学认为,上述反应的生成物可能与反应温度(T),KOH溶液的浓度(C)有关.他们做了如下对比实验(每次反应中硫粉的质量、KOH溶液的体积均相同).
| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| T/℃ | 50 | 60 | 70 | 80 | 90 | |||
| c/mol•L-1 | 1.0 | 3.0 | 4.0 | 5.0 | 6.0 |
(2)兴趣小组设计实验对上述反应中生成的盐的成分进行探究.他们提出如下假设,请你根据氧化还原反应的规律,完成假设二和假设三:
假设一:生成的盐是K2S和K2SO3;
假设二:生成的盐是K2S和K2SO4;
假设三:生成的盐是K2S,K2SO3和K2SO4;
(3)请你设计实验验证上述假设一.完成下表中内容.(除了硫粉与热的KOH溶液的反应液之外,可供选择的药品有稀硝酸,稀盐酸等;已知:6H++SO32-+2S2-=3S+3H2O)
| 实验方案(不要求写出具体操作过程) | 预期实验现象和结论 |
| 在反应液中加入足量的稀盐酸 | 若溶液变浑浊且没有气体溢出(或:若没有气体溢出),则假设一成立;若溶液中有气体逸出,则假设一不成立 |
(5)请分析上述反应中有K2SO4生成的可能原因是:亚硫酸钾具有还原性,很容易被氧气氧化为硫酸钾.
6.下列反应中,反应后固体物质的质量不变的是( )
| A. | 氢气通过灼热的氧化铜 H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | |
| B. | 二氧化碳通过Na2O2粉末 2Na2O2+2CO2═2Na2CO3+O2 | |
| C. | 铝与Fe2O3发生铝热反应 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | |
| D. | 将锌粒投入Cu(NO3)2溶液 Zn+Cu(NO3)2═Zn(NO3)2+Cu |
2.下列反应中溶液中的H+浓度显著增大的是( )
| A. | 将SO2通入品红溶液中 | B. | 将Cl2通入KI溶液中 | ||
| C. | 将SO2通入溴水中 | D. | 将H2S通入硝酸溶液中 |
1.在热的稀H2SO4溶液中溶解了11.4g FeSO4,当加入50mL 0.5mol/L KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也反应完全,并有NxOy气体逸出:
□FeSO4+□KNO3+□H2SO4→K2SO4+□Fe2(SO4)3+□NxOy+□H2O
据此推算出x、y的值分别为( )
0 172007 172015 172021 172025 172031 172033 172037 172043 172045 172051 172057 172061 172063 172067 172073 172075 172081 172085 172087 172091 172093 172097 172099 172101 172102 172103 172105 172106 172107 172109 172111 172115 172117 172121 172123 172127 172133 172135 172141 172145 172147 172151 172157 172163 172165 172171 172175 172177 172183 172187 172193 172201 203614
□FeSO4+□KNO3+□H2SO4→K2SO4+□Fe2(SO4)3+□NxOy+□H2O
据此推算出x、y的值分别为( )
| A. | 1、2 | B. | 1、1 | C. | 2、1 | D. | 2、3 |
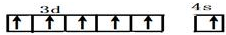 ,B在元素周期表的位置第二周期第ⅣA族
,B在元素周期表的位置第二周期第ⅣA族 A、B、C、D、E、F六种物质在一定条件下有如图所示的相互转化关系,所有反应物和生成物均已给出.
A、B、C、D、E、F六种物质在一定条件下有如图所示的相互转化关系,所有反应物和生成物均已给出. 下面是有关物质的转化关系图(部分产物已省略),其中A为单质,E在常温下为液体,D是一种气体,C的相对分子质量为78.请回答下列有关问题:
下面是有关物质的转化关系图(部分产物已省略),其中A为单质,E在常温下为液体,D是一种气体,C的相对分子质量为78.请回答下列有关问题: ;G→H的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
;G→H的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.