题目内容
3.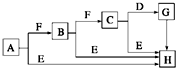 下面是有关物质的转化关系图(部分产物已省略),其中A为单质,E在常温下为液体,D是一种气体,C的相对分子质量为78.请回答下列有关问题:
下面是有关物质的转化关系图(部分产物已省略),其中A为单质,E在常温下为液体,D是一种气体,C的相对分子质量为78.请回答下列有关问题:(1)下列对C的结构、性质推断中不正确的是D.
A.久置于空气中会变成白色 B.具有强氧化性
C.晶体中存在离子键与共价键 D.是一种碱性氧化物
(2)A的原子结构示意图为
 ;G→H的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
;G→H的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.(3)C和E反应生成H的离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑,反应中氧化剂与还原剂的物质的量之比为1:1.
分析 A为单质,A能与F发生连续反应生成C,C的相对分子质量为78,可推知A为Na,F为O2,B为Na2O,C为Na2O2,E在常温下为液体,则E为H2O,钠与水、氧化钠与水、过氧化钠与水都产生氢氧化钠,所以H为NaOH,D是一种气体,则D为CO2,与过氧化钠反应生成G为Na2CO3,G与氢氧化钙反应生成氢氧化钠,符合各物质的转化关系,据此答题.
解答 解:A为单质,A能与F发生连续反应生成C,C的相对分子质量为78,可推知A为Na,F为O2,B为Na2O,C为Na2O2,E在常温下为液体,则E为H2O,钠与水、氧化钠与水、过氧化钠与水都产生氢氧化钠,所以H为NaOH,D是一种气体,则D为CO2,与过氧化钠反应生成G为Na2CO3,G与氢氧化钙反应生成氢氧化钠,符合各物质的转化关系,
(1)C为Na2O2,
A.Na2O2久置于空气中会变成生成碳酸钠,为白色固体,故A正确;
B.Na2O2具有强氧化性,故B正确;
C.Na2O2晶体中存在离子键与共价键,故C正确;
D.Na2O2不是一种碱性氧化物,故D错误,
故答案为:D;
(2)A为Na,A的原子结构示意图为 ,G→H的化学方程式 Na2CO3+Ca(OH)2═Ca CO3↓+2 NaOH,
,G→H的化学方程式 Na2CO3+Ca(OH)2═Ca CO3↓+2 NaOH,
故答案为: ;Na2CO3+Ca(OH)2═Ca CO3↓+2 NaOH;
;Na2CO3+Ca(OH)2═Ca CO3↓+2 NaOH;
(3)C和E反应生成H的反应为Na2O2与H2O反应生成氢氧化钠与氢气,离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑,反应中氧化剂与还原剂的物质的量之比为1:1,
故答案为:2Na2O2+2H2O═4Na++4OH-+O2↑;1:1.
点评 本题考查无机物的推断,题目难度不大,本题注意把握常见物质的相互转化,为解答该题的关键,注意把握相关物质的性质,学习中注意积累.

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案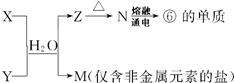 表为元素周期表的一部分,请参照元素①-⑨在表中的位置,回答下列问题:
表为元素周期表的一部分,请参照元素①-⑨在表中的位置,回答下列问题: | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑨ | ⑥ | ⑦ | ⑧ |
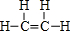 ,该物质与溴水发生加成反应的化学方程式是CH2=CH2+Br2→BrCH2CH2Br.
,该物质与溴水发生加成反应的化学方程式是CH2=CH2+Br2→BrCH2CH2Br.(2)用电子式表示④的简单氢化物的形成过程
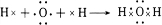
(3)用①元素的单质与④元素的单质可以制成原电池,电池中装有KOH浓溶液,将多孔的惰性电极甲和乙浸入KOH溶液中,在甲极通入①的单质,乙极通入④的单质,则甲极的电极反应式为:H2-2e-+2OH-=2H2O
(4)由表中①、③、④、⑥、⑧元素形成的常见物质X、Y、Z、M、N可发生(如图)反应:
X溶液与Y溶液反应的离子方程式为Al3++3NH3.3H2O=Al(OH)3↓+3NH4+,工业上常用单质⑥冶炼难熔的金属,写出氧化铁和单质⑥在高温下反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
| A. | 1:1:1:1 | B. | 2:2:1:2 | C. | 1:3:1:1 | D. | 4:3:2:1 |
| A. | 将40g NaOH固体溶解于1L水中 | |
| B. | 将22.4L氯化氢气体溶于水配成lL溶液 | |
| C. | 将1L 10mol/L的浓盐酸与9L水混合 | |
| D. | 20g NaOH固体溶解在水中配成500mL溶液 |
| A. | Br-、Cl-、I- | B. | Cl-、I-、Br- | C. | I-、Br-、Cl- | D. | Br-、I-、Cl- |
①X元素原子的价电子排布式为ns1,且原子半径是同族元素最小的.
②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布式中,p轨道上只有1个未成对电子.
③Z元素的电离能(用符号I表示)数据见表(kJ•mol-1)
| I1 | I2 | I3 | I4 | … |
| 496 | 4 562 | 6 912 | 9 540 | … |
(1)Z2Y中含有的化学键类型为离子键.
(2)Z2Y2的电子式为
 .
.(3)X2Y分子的空间构型为V形,其中心原子的杂化方式为sp3,XWY属于极性(填“极性”或“非极性”)分子.
 如图为实验室蒸馏自来水得到少量蒸馏水的装置示意图如图2,请根据图示回答下列问题:
如图为实验室蒸馏自来水得到少量蒸馏水的装置示意图如图2,请根据图示回答下列问题: