题目内容
2.下列反应中溶液中的H+浓度显著增大的是( )| A. | 将SO2通入品红溶液中 | B. | 将Cl2通入KI溶液中 | ||
| C. | 将SO2通入溴水中 | D. | 将H2S通入硝酸溶液中 |
分析 反应中溶液中的H+浓度显著增大,说明二者反应时生成物中能电离出大量氢离子,据此分析解答.
解答 解:A.SO2能和有色物质品红溶液反应生成无色物质而体现漂白性,溶液中氢离子浓度变化不明显,故A不选;
B.该反应方程式为Cl2+2KI=I2+2KCl,溶液仍然呈中性,氢离子浓度变化不大,故B不选;
C.发生的反应为SO2+2Br2+2H2O=2HBr+H2SO4,溶液由强酸生成,导致溶液中氢离子浓度显著增大,故C选;
D.发生的反应为3H2S+2HNO3=2NO+4H2O+3S,溶液中氢离子浓度减小,故D不选;
故选C.
点评 本题考查元素化合物性质,为高频考点,明确物质之间反应及物质性质是解本题关键,注意CD中发生的反应,为易错点.

练习册系列答案
相关题目
12.请从“实验现象”栏中选择正确选项的字母代号填入“答案”栏中.
| 实 验 操 作 | 答案 | 实验现象 |
| (1)向鸡蛋清中滴加少许浓硝酸,微热 | B | A.紫色褪去 B.变黄色 C.出现蓝色 D.溶液分层,下层呈紫红色 |
| (2)将乙烯通入少量酸性KMnO4溶液中 | A | |
| (3)将CCl4滴入盛有碘水的试管中,充分振荡,静止 | D | |
| (4)向土豆片上滴加碘水 | C |
10.NA表示阿伏加德罗常数,下列说法不正确的是( )
| A. | H2SO4的摩尔质量(g/mol)与NA个硫酸分子的质量(g)在数值上相等 | |
| B. | NA个氧气分子和NA个氮气分子的质量比为8:7 | |
| C. | 1mol•L-1 CaCl2溶液中所含Ca2+离子的数目为NA | |
| D. | 1mol D2(重氢分子)中含有2NA个中子 |
7.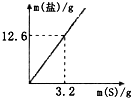 资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.
资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.
(1)兴趣小组同学认为,上述反应的生成物可能与反应温度(T),KOH溶液的浓度(C)有关.他们做了如下对比实验(每次反应中硫粉的质量、KOH溶液的体积均相同).
实验①~④是探究温度对生成物的影响,⑤~⑧是探究KOH溶液的浓度对生成物的影响.请在表中相应空格填入相应数据.
(2)兴趣小组设计实验对上述反应中生成的盐的成分进行探究.他们提出如下假设,请你根据氧化还原反应的规律,完成假设二和假设三:
假设一:生成的盐是K2S和K2SO3;
假设二:生成的盐是K2S和K2SO4;
假设三:生成的盐是K2S,K2SO3和K2SO4;
(3)请你设计实验验证上述假设一.完成下表中内容.(除了硫粉与热的KOH溶液的反应液之外,可供选择的药品有稀硝酸,稀盐酸等;已知:6H++SO32-+2S2-=3S+3H2O)
(4)兴趣小组通过改变硫粉的质量,得出生成钾盐的质量与硫粉质量的变化关系如图所示.有人据此得出结论:生成的盐一定是K2S和K2SO3的混合物.请你根据计算结果指出该结论是否正确:不正确.
(5)请分析上述反应中有K2SO4生成的可能原因是:亚硫酸钾具有还原性,很容易被氧气氧化为硫酸钾.
 资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.
资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.(1)兴趣小组同学认为,上述反应的生成物可能与反应温度(T),KOH溶液的浓度(C)有关.他们做了如下对比实验(每次反应中硫粉的质量、KOH溶液的体积均相同).
| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| T/℃ | 50 | 60 | 70 | 80 | 90 | |||
| c/mol•L-1 | 1.0 | 3.0 | 4.0 | 5.0 | 6.0 |
(2)兴趣小组设计实验对上述反应中生成的盐的成分进行探究.他们提出如下假设,请你根据氧化还原反应的规律,完成假设二和假设三:
假设一:生成的盐是K2S和K2SO3;
假设二:生成的盐是K2S和K2SO4;
假设三:生成的盐是K2S,K2SO3和K2SO4;
(3)请你设计实验验证上述假设一.完成下表中内容.(除了硫粉与热的KOH溶液的反应液之外,可供选择的药品有稀硝酸,稀盐酸等;已知:6H++SO32-+2S2-=3S+3H2O)
| 实验方案(不要求写出具体操作过程) | 预期实验现象和结论 |
| 在反应液中加入足量的稀盐酸 | 若溶液变浑浊且没有气体溢出(或:若没有气体溢出),则假设一成立;若溶液中有气体逸出,则假设一不成立 |
(5)请分析上述反应中有K2SO4生成的可能原因是:亚硫酸钾具有还原性,很容易被氧气氧化为硫酸钾.
14.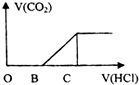 向某NaOH溶液中通入CO2气体后 得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示.则下列分析与判断正确的是(不计CO2溶解)( )
向某NaOH溶液中通入CO2气体后 得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示.则下列分析与判断正确的是(不计CO2溶解)( )
 向某NaOH溶液中通入CO2气体后 得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示.则下列分析与判断正确的是(不计CO2溶解)( )
向某NaOH溶液中通入CO2气体后 得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示.则下列分析与判断正确的是(不计CO2溶解)( )| A. | 若OB=0,则溶液M为Na2CO3溶液 | |
| B. | 若OB=BC,则形成溶液M所发生反应的离子方程式为OH-+CO2═HCO3- | |
| C. | 若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3) | |
| D. | 若OB>BC,则溶液M中大量存在的阴离子为CO32-和HCO3- |
11.下列说法正确的是( )
| A. | 14C与 12C互称同位素;O2与O3是氧元素的同素异形体 | |
| B. | 钢铁生锈主要发生吸氧腐蚀,镀锌铁皮镀层破损后对铁失去保护作用 | |
| C. | 石油的分馏、煤的干馏、电解质溶液导电均属于物理变化 | |
| D. | SO2和NO2属于酸性氧化物,Na2O和Fe3O4属于碱性氧化物 |
19.几种短周期元素的原子半径及常见化合价见表:
请分析上表中有关数据,并结合已学知识,回答以下问题(涉及上述元素的答案,请用元素符号表示):
(1)E元素在周期表中位置是第二周期IA族.
(2)A、H、J对应离子的半径由大到小的顺序是F->Na+>Al3+(填离子符号)
(3)A与J所形成的化合物中含有离子键(填“离子”或“共价”)
(4)写出DB2的电子式: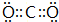 .
.
(5)写出D的最高价氧化物与J的最高价氧化物对应水化物X的溶液(足量)发生反应的离子方程式:CO2+OH-=HCO3-.
| 元素代号 | A | B | C | D | E | F | G | H | I | J | K |
| 常见化合价 | -1 | -2 | +5、-3 | +4、-4 | +6、+4、-2 | +4、-4 | +5、-3 | +3 | +2 | +1 | +1 |
| 原子半径/pm | 71 | 74 | 75 | 77 | 102 | 117 | 110 | 143 | 160 | 186 | 152 |
(1)E元素在周期表中位置是第二周期IA族.
(2)A、H、J对应离子的半径由大到小的顺序是F->Na+>Al3+(填离子符号)
(3)A与J所形成的化合物中含有离子键(填“离子”或“共价”)
(4)写出DB2的电子式:
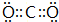 .
.(5)写出D的最高价氧化物与J的最高价氧化物对应水化物X的溶液(足量)发生反应的离子方程式:CO2+OH-=HCO3-.
