5.下列说法正确的是( )
| A. | 某微粒核外电子排布为2、8、8结构,则该微粒一定是氩原子 | |
| B. | 最外层达稳定结构的微粒只能是稀有气体的原子 | |
| C. | F-、Na+、Ca2+、Al3+是与Ne原子具有相同电子层结构的离子 | |
| D. | NH4+与H3O+具有相同的质子数和电子数 |
4.有四种溶液,它们分别含有S2-、HCO3-、Al3+、Fe2+四种离子,若向其中分别先加入足量Na2O2后,再通入过量HCl气体,溶液中离子数目基本保持不变的是( )
| A. | S2- | B. | HCO3- | C. | Al3+ | D. | Fe2+ |
3.NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| B. | 2L0.5mol/L碳酸钠溶液中含有的CO32-数为NA | |
| C. | 标准状况下22.4LH2O的分子数为NA | |
| D. | 18gD2O和18gH2O中含有的电子数均为10NA |
2.某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1 盐酸、0.55mol•L-1NaOH溶液,
尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
已知:Q=Cm(t2-t1),反应后溶液的比热容C为4.18KJ•℃-1•Kg-1,各物质的密度均为1g•cm-3.计算完成上表.
(4)实验中NaOH的浓度比HCl的大,其原因是确保盐酸完全反应,使反应更充分
(5)若用KOH代替NaOH,对测定结果无(填“有”或“无”)影响;若用醋酸代替HCl做实验,则测定结果偏低(填“偏高”“偏低”或“无影响”).
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1 盐酸、0.55mol•L-1NaOH溶液,
尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
| 实 验 用 品 | 溶 液 温 度 | 中和热 △H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
(4)实验中NaOH的浓度比HCl的大,其原因是确保盐酸完全反应,使反应更充分
(5)若用KOH代替NaOH,对测定结果无(填“有”或“无”)影响;若用醋酸代替HCl做实验,则测定结果偏低(填“偏高”“偏低”或“无影响”).
19.下列性质的比较中,正确的是( )
0 171236 171244 171250 171254 171260 171262 171266 171272 171274 171280 171286 171290 171292 171296 171302 171304 171310 171314 171316 171320 171322 171326 171328 171330 171331 171332 171334 171335 171336 171338 171340 171344 171346 171350 171352 171356 171362 171364 171370 171374 171376 171380 171386 171392 171394 171400 171404 171406 171412 171416 171422 171430 203614
| A. | 碱性:KOH>NaOH>Mg(OH)2>Ca(OH)2 | B. | 沸点:HF<HCl<HBr<HI | ||
| C. | 热稳定性:CH4>PH3>H2O>HF | D. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
 某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu元素的相对原子质量为64).按照实验步骤依次回答下列问题:
某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu元素的相对原子质量为64).按照实验步骤依次回答下列问题: 如图1是一套实验室制取乙烯验证乙烯具有还原性的实验装置,请回答:
如图1是一套实验室制取乙烯验证乙烯具有还原性的实验装置,请回答:
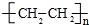 ,该反应属于加聚反应;
,该反应属于加聚反应;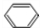 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$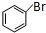 +HBr.
+HBr. 、
、 、
、 、
、 .
.