题目内容
17.根据图示填空:
(1)化合物A含有的官能团碳碳双键;
(2)反应①的化学反应方程式是HC≡CH+H2$→_{△}^{Ni}$CH2=CH2,该反应属于加成反应;
(3)反应②的化学方程式n CH2=CH2$→_{△}^{催化剂}$
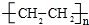 ,该反应属于加聚反应;
,该反应属于加聚反应;(4)反应④的化学方程式
 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$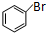 +HBr.
+HBr.
分析 乙炔转化得到A,A可以得到聚乙烯,则乙炔与氢气发生加成反应生成A为乙烯,乙烯发生加聚反应生成聚乙烯,乙炔发生加成反应得到苯,苯与溴发生取代反应得到B为溴苯.
解答 解:乙炔转化得到A,A可以得到聚乙烯,则乙炔与氢气发生加成反应生成A为乙烯,乙烯发生加聚反应生成聚乙烯,乙炔发生加成反应得到苯,苯与溴发生取代反应得到B为溴苯.
(1)化合物A为乙烯,含有的官能团为:碳碳双键,故答案为:碳碳双键;
(2)反应①的化学反应方程式是:HC≡CH+H2$→_{△}^{Ni}$CH2=CH2,该反应属于加成反应,
故答案为:HC≡CH+H2$→_{△}^{Ni}$CH2=CH2;加成;
(3)反应②的化学方程式:n CH2=CH2$→_{△}^{催化剂}$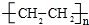 ,该反应属于加聚反应,
,该反应属于加聚反应,
故答案为:n CH2=CH2$→_{△}^{催化剂}$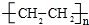 ;加聚;
;加聚;
(4)反应④的化学方程式: +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr,
+HBr,
故答案为: +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr.
+HBr.
点评 本题考查有机物的推断,涉及不饱和烃的性质与转化,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
7.下列各组液体混合物,用分液漏斗能分开的是( )
| A. | 乙醛和水 | B. | 苯和硝基苯 | C. | 乙酸乙酯和水 | D. | 溴乙烷和氯仿 |
8.下列物质中不能由单质直接化合生成的是( )
①CuS ②FeS ③SO3 ④Fe2O3 ⑤FeCl2⑥Hg2S.
①CuS ②FeS ③SO3 ④Fe2O3 ⑤FeCl2⑥Hg2S.
| A. | ①②③⑤ | B. | ①③⑤⑥ | C. | ①③④⑤⑥ | D. | .全部 |
5. “低碳循环”、如何降低大气中CO2的含量、有效地开发利用CO2,引起了全世界的普遍重视.
“低碳循环”、如何降低大气中CO2的含量、有效地开发利用CO2,引起了全世界的普遍重视.
I. 用电弧法合成的储氢纳米碳管,可用如下氧化法提纯,请完成下述反应:
5 C+4 KMnO4+6 H2SO4→5CO2↑+4MnSO4+2K2SO4+6 H2O
II.某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,得到如表数据:
(1)实验I中,前5min的反应速率υ(CO2)=0.1mol•L-1•min-1.
(2)下列能判断在800℃实验条件下CO(g)与H2O(g)反应一定达到平衡状态的是D.
A.容器内压强不再变化 B.$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$=2
C.混合气体密度不变 D.υ正(CO)=υ逆(CO2)
(3)实验III中:y=1.
(4)Ⅲ的若实验容器改为在绝热的密闭容器中进行,实验测得H2O(g)的转化率a(H2O)随时间变化的示意图,如图所示,b点:υ正>υ逆(填“<”.“=”或“>”).
 “低碳循环”、如何降低大气中CO2的含量、有效地开发利用CO2,引起了全世界的普遍重视.
“低碳循环”、如何降低大气中CO2的含量、有效地开发利用CO2,引起了全世界的普遍重视.I. 用电弧法合成的储氢纳米碳管,可用如下氧化法提纯,请完成下述反应:
5 C+4 KMnO4+6 H2SO4→5CO2↑+4MnSO4+2K2SO4+6 H2O
II.某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,得到如表数据:
| 实验组 | 温度/℃ | 起始量(mol) | 平衡量(mol) | 达到平衡所需要时间/min | ||
| CO(g) | H2O(g) | CO2(g) | H2(g) | |||
| I | 800 | 2 | 2 | x | 1 | 5 |
| II | 900 | 1 | 2 | 0.5 | 0.5 | tm |
| III | 900 | 2 | 4 | y | y | tn |
(2)下列能判断在800℃实验条件下CO(g)与H2O(g)反应一定达到平衡状态的是D.
A.容器内压强不再变化 B.$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$=2
C.混合气体密度不变 D.υ正(CO)=υ逆(CO2)
(3)实验III中:y=1.
(4)Ⅲ的若实验容器改为在绝热的密闭容器中进行,实验测得H2O(g)的转化率a(H2O)随时间变化的示意图,如图所示,b点:υ正>υ逆(填“<”.“=”或“>”).
12.下列说法正确的是( )
| A. | 新戊烷的一氯取代物有两种 | |
| B. | 异丁烷的一氯取代物有两种 | |
| C. | 同分异构体只存在于有机物中 | |
| D. | 相对分子质量相同,结构式不同的物质互称同分异构体 |
2.某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1 盐酸、0.55mol•L-1NaOH溶液,
尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
已知:Q=Cm(t2-t1),反应后溶液的比热容C为4.18KJ•℃-1•Kg-1,各物质的密度均为1g•cm-3.计算完成上表.
(4)实验中NaOH的浓度比HCl的大,其原因是确保盐酸完全反应,使反应更充分
(5)若用KOH代替NaOH,对测定结果无(填“有”或“无”)影响;若用醋酸代替HCl做实验,则测定结果偏低(填“偏高”“偏低”或“无影响”).
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L-1 盐酸、0.55mol•L-1NaOH溶液,
尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
| 实 验 用 品 | 溶 液 温 度 | 中和热 △H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
(4)实验中NaOH的浓度比HCl的大,其原因是确保盐酸完全反应,使反应更充分
(5)若用KOH代替NaOH,对测定结果无(填“有”或“无”)影响;若用醋酸代替HCl做实验,则测定结果偏低(填“偏高”“偏低”或“无影响”).
9.下列说法正确的是( )
| A. | 离子化合物不可以含共价键 | |
| B. | 含有共价键的化合物不一定是共价化合物,但是共价化合物只能含有共价键 | |
| C. | 共价化合物可以含离子键 | |
| D. | 离子键、共价键、金属键和氢键都是化学键 |
7.下列盛放试剂的方法正确的是( )
| A. | 液态溴有毒且易挥发,应贮存于磨口的细口瓶中,加水封,加盖橡胶塞,并放置于阴凉处 | |
| B. | 汽油或煤油存放在带橡胶塞的棕色玻璃瓶中 | |
| C. | 碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中 | |
| D. | 氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中 |