题目内容
20.已知:2H2( g )+O2( g )═2H2O ( l )△H═-571.6kJ/mol2H2( g )+O2( g )═2H2O ( g )△H═-483.6kJ/mol
CH4 ( g )+2O2( g )═2H2O ( l )+CO2( g )△H═-890kJ/mol
常温下,取甲烷和氢气的混合气体11.2L(标准状况下)经完全燃烧后恢复到常温,则放出的热量为64.18kJ,试求混合气体中甲烷和氢气体积比.
分析 甲烷和氢气的混合气体11.2L(标准状况下),则其物质的量为0.5mol,设甲烷为xmol,氢气为ymol,根据物质的量之比等于热量比,结合热化学方程式计算.
解答 解:甲烷和氢气的混合气体11.2L(标准状况下),则其物质的量为0.5mol,设甲烷为xmol,氢气为ymol,
已知:2H2(g)+O2(g)=2H2O (l)△H=-571.6kJ/mol
2H2(g)+O2(g)=2H2O (g)△H=-483.6kJ/mol
CH4 (g)+2O2(g)=2H2O (l)+CO2(g)△H=-890kJ/mol
常温下,水为液态,则xmol甲烷燃烧放出的热量为890xkJ,ymol氢气燃烧放出热量为$\frac{y}{2}$×571.6kJ,
所以890xkJ+$\frac{y}{2}$×571.6kJ=64.18kJ,
x+y=0.5mol
解得:$\frac{x}{y}$=$\frac{59}{100}$,
答:混合气体中甲烷和氢气体积比为$\frac{59}{100}$.
点评 本题考查根据热化学方程式进行的有关反应热的计算,难度不大,理解热化学方程式的意义是关键,注意室温下水为液体.

练习册系列答案
相关题目
10.下列说法正确的是( )
| A. | 煤的液化、气化是物理变化,煤的干馏是化学变化 | |
| B. | 蛋白质、淀粉、纤维素、油脂均属于高分子化合物 | |
| C. | 乙酸乙酯在碱性条件下的水解反应属于皂化反应 | |
| D. | 石油裂化的目的是为了提高汽油等轻质液态油的产量和质量 |
11.下列除去杂质的方法中错误的是( )
| 物质 | 杂质 | 除杂质的方法 | |
| A | SiO2 | CaCO3 | 过量稀硫酸、过滤 |
| B | 铜粉 | 铝粉 | 过量CuCl2溶液、过滤 |
| C | FeCl3溶液 | FeCl2 | 通入适量氯气 |
| D | SO2 | HC1 | 通过NaHSO3溶液的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
8.下列说法正确的是( )
| A. | 只能从动植物等有机体中取得的化合物称为有机物 | |
| B. | 乙烯、苯、环己烷都属于脂肪烃 | |
| C. | 含有苯环的有机物称为芳香烃 | |
| D. | 仅含碳氢元素的有机化合物称为烃 |
5.下列说法正确的是( )
| A. | 某微粒核外电子排布为2、8、8结构,则该微粒一定是氩原子 | |
| B. | 最外层达稳定结构的微粒只能是稀有气体的原子 | |
| C. | F-、Na+、Ca2+、Al3+是与Ne原子具有相同电子层结构的离子 | |
| D. | NH4+与H3O+具有相同的质子数和电子数 |
12. 单质硼有无定形和晶体两种,参考下表数据
单质硼有无定形和晶体两种,参考下表数据
(1)晶体硼的晶体类型属于原子晶体,理由是熔、沸点很高、硬度很大.
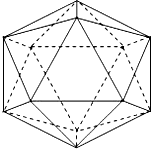
(2)已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个项点上各有1个B原子.通过视察图形及推算,此晶体体结构单元由12个硼原子构成.其中B-B键的键角为60°.共含有30个B-B.
 单质硼有无定形和晶体两种,参考下表数据
单质硼有无定形和晶体两种,参考下表数据| 金刚石 | 晶体硅 | 晶体硼 | |
| 熔点 | 3823 | 1683 | 2573 |
| 沸点 | 5100 | 2628 | 2823 |
| 硬度 | 10 | 7.0 | 9.5 |
(2)已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个项点上各有1个B原子.通过视察图形及推算,此晶体体结构单元由12个硼原子构成.其中B-B键的键角为60°.共含有30个B-B.
10.下列设备工作过程中,将电能转化为化学能的是( )
| A. |  充电器给手机充电 | B. |  太阳能交通信号灯 | ||
| C. |  电饭煲煮饭 | D. |  天然气汽车 |
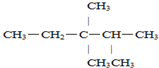 2,3,3-三甲基戊烷;
2,3,3-三甲基戊烷;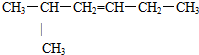 2-甲基-3-己烯;
2-甲基-3-己烯;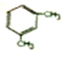 1,3-二甲基苯.(用系统命名法命名)
1,3-二甲基苯.(用系统命名法命名) A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题: