题目内容
5.下列说法正确的是( )| A. | 某微粒核外电子排布为2、8、8结构,则该微粒一定是氩原子 | |
| B. | 最外层达稳定结构的微粒只能是稀有气体的原子 | |
| C. | F-、Na+、Ca2+、Al3+是与Ne原子具有相同电子层结构的离子 | |
| D. | NH4+与H3O+具有相同的质子数和电子数 |
分析 A.某微粒核外电子排布为2、8、8结构,则该微粒可能为氩原子、钾离子、氯离子等;
B.最外层达稳定结构的微粒可能为阳离子或阴离子;
C.若核外电子数相同,则电子层结构相同;
D.NH4+与H3O+均含有11个质子、10个电子.
解答 解:A.某微粒核外电子排布为2、8、8结构,则该微粒可能为氩原子、钾离子、氯离子等,故A错误;
B.最外层达稳定结构的微粒可能为阳离子或阴离子,如钠离子、硫离子,故B错误;
C.F-、Na+、Al3+与Ne原子核外均含有10个电子,具有相同电子层结构,但Ca2+核外有18个电子,与Ne原子电子层结构不相同,故C错误;
D.NH4+与H3O+均含有11个质子、10个电子,故D正确,
故选:D.
点评 本题考查核外电子排布、原子构成等,比较基础,注意利用列举法解答.

练习册系列答案
相关题目
15. 如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
 如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )| a | b | c | |
| A | AlCl3 | NaAlO2 | Al(OH)3 |
| B | NaOH | Na2CO3 | NaHCO3 |
| C | Fe | FeCl3 | FeCl2 |
| D | Si | SiO2 | H2SiO3 |
| A. | A | B. | B | C. | C | D. | D |
16.金刚石和石墨是碳元素的两种结构不同的单质(同素异形体).在100kPa时,1molC(石墨)转化为金刚石,要吸收1.895kJ的热能.据此,试判断在100kPa压强下,下列结论正确的是( )
| A. | 石墨和金刚石一样稳定 | |
| B. | 金刚石比石墨稳定 | |
| C. | 1 mol C(石墨)比1 mol C(金刚石)的总能量高 | |
| D. | 1 mol C(石墨)比1 mol C(金刚石)的总能量低 |
13.下列有机物命名正确的是( )
| A. | 2-乙基丁烷 | B. | 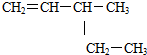 ;3-乙基-1-丁烯 ;3-乙基-1-丁烯 | ||
| C. | 2,6-二甲基-3-乙基庚烷 | D. | CH2=CH-CH=CH2;1,3,5-三己烯 |
10.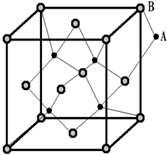 如图所示晶体中每个阳离子A或阴离子B,均可被另一种离子以四面体形式包围着,则该晶体对应的化学式为( )
如图所示晶体中每个阳离子A或阴离子B,均可被另一种离子以四面体形式包围着,则该晶体对应的化学式为( )
 如图所示晶体中每个阳离子A或阴离子B,均可被另一种离子以四面体形式包围着,则该晶体对应的化学式为( )
如图所示晶体中每个阳离子A或阴离子B,均可被另一种离子以四面体形式包围着,则该晶体对应的化学式为( )| A. | AB | B. | A2B | C. | AB3 | D. | A2B3 |
15.下列物质的分类合理的是( )
| A. | 碱性氧化物:Na2O、CO、Al2O3、Na2O2 | B. | 碱:NaOH、KOH、Ba(OH)2、Na2CO3 | ||
| C. | 氧化物:Fe2O3、NO、SO2、H2O | D. | 电解质:KNO3、Cl2、HCl、BaSO4 |

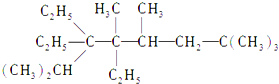 2,2,4,5,7,7-六甲基-3,3,4-乙基辛烷,
2,2,4,5,7,7-六甲基-3,3,4-乙基辛烷,