题目内容
16.填空:(1)某烷烃的蒸气密度是2.59g/L(标准状况下)该烷烃的分子式为C4H8,该烷烃的结构简式可能为CH3CH2CH2CH3、CH(CH3)3.
(2)某气态烷烃20mL,完全燃烧时,正好消耗同温同压下的氧气100mL,该烃的分子为C3H8.
(3)分子式为C4H8的烯烃有3种同分异构体(不考虑立体异构).
(4)分子式为C5H8的炔烃有3种同分异构体,分别写出其结构简式CH≡CCH2CH2CH3、CH3C≡CCH2CH3、CH≡CCH(CH3)2.
(5)分子式为C8H10的芳香烃有4种同分异构体,分别写出其结构简式
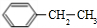 、
、 、
、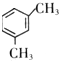 、
、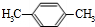 .
.
分析 (1)根据M=ρVm计算烷烃的摩尔质量,再根据烷烃组成通式CnH2n+2确定分子式,书写可能的结构简式;
(2)烷烃分子式为式CnH2n+2,结合含氧量计算n的值;
(3)分子式为C4H8的烯烃,不考虑立体异构,考虑官能团位置异构、碳链异构;
(4)分子式为C5H8的炔烃有官能团位置异构、碳链异构;
(5)分子式为C8H10的芳香烃有乙苯、二甲苯.
解答 解:(1)烷烃的摩尔质量为2.59g/L×22.4L/mol=58g/mol,烷烃分子式为CnH2n+2,则14n+2=58,解得n=4,故该烷烃的分子式为C4H8,可能的结构简式有:CH3CH2CH2CH3、CH(CH3)3,
故答案为:C4H8;CH3CH2CH2CH3、CH(CH3)3;
(2)烷烃分子式为式CnH2n+2,气态烷烃20mL完全燃烧时,正好消耗同温同压下的氧气100mL,则20×(n+$\frac{2n+2}{4}$)=100,解得n=3,故该烷烃分子式为:C3H8,
故答案为:C3H8;
(3)分子式为C4H8的烯烃,不考虑立体异构,可能的结构简式有:CH2=CHCH2CH3、CH3CH=CHCH3、CH2=C(CH3)2,
故答案为:3;
(4)分子式为C5H8的炔烃,可能的结构简式有:CH≡CCH2CH2CH3、CH3C≡CCH2CH3、CH≡CCH(CH3)2,
故答案为:3;CH≡CCH2CH2CH3、CH3C≡CCH2CH3、CH≡CCH(CH3)2;
(5)分子式为C8H10的芳香烃有乙苯、二甲苯,可能的结构简式有: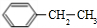 、
、 、
、 、
、 ,
,
故答案为:4;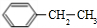 、
、 、
、 、
、 .
.
点评 本题考查有机物分子式确定、同分异构体的书写,难度不大,侧重对基础知识的巩固.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列应用不涉及氧化还原反应的是( )
| A. | 工业上用石灰乳与氯气制漂白粉 | B. | 工业上电解熔融状态Al2O3制备Al | ||
| C. | 工业上利用合成氨实现人工固氮 | D. | 自来水厂用明矾做净水剂 |
4.下列离子方程式中正确的是( )
| A. | 向碳酸钠溶液中加入足量的盐酸 CO32-+2H+═CO2↑+H2O | |
| B. | 单质铁和三氯化铁溶液反应生成氯化亚铁 Fe+Fe3+═2Fe2+ | |
| C. | 金属钠与水反应生成氢氧化钠和氢气 Na+H2O═Na++OH-+H2↑ | |
| D. | 氯化铵晶体和石灰粉共热产生氨气 NH4++OH-═NH3↑+H2O |
11.下列说法正确的是( )
| A. | C3H6和C4H8一定是同系物 | B. | D和T是同素异形体 | ||
| C. | C2H6和C10H22一定是同系物 | D. | 金刚石和石墨是同位素 |
8.能够用键能解释的是( )
| A. | 氮气的化学性质比氧气稳定 | B. | 常温常压下,溴呈液体,碘为固体 | ||
| C. | 稀有气体一般很难发生化学反应 | D. | 硝酸易挥发,硫酸难挥发 |
5.下列物质性质的变化规律与分子间作用力有关的是( )
| A. | F2、CI2、Br2、I2的熔、沸点逐渐升高 | |
| B. | 碳化硅、晶体硅的熔、沸点很高 | |
| C. | NaF、NaCI、NaBr、NaI的熔点依次降低 | |
| D. | HF、HCI、HBr、HI的热稳定性依次 |
6.要配制浓度约为2mol/LNaOH溶液100mL,下面的操作正确的是( )
| A. | 称取8gNaOH固体,放入100mL量筒,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL | |
| B. | 称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 | |
| C. | 称取8gNaOH固体放入300mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 | |
| D. | 用50mL量筒量取50mL4mol/LNaOH溶液,倒入100mL烧杯中,再用同一量筒取50mL蒸馏水,不断搅拌下,慢慢倒入烧杯中 |
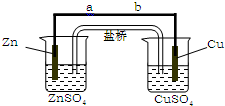 某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu元素的相对原子质量为64).按照实验步骤依次回答下列问题:
某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu元素的相对原子质量为64).按照实验步骤依次回答下列问题: