17.一定条件下,发生反应:①M(s)+N(g)?R(g)△H=-Q1kJ•mol-1,②2R (g)+N(g)?2T (g)
△H=-Q2kJ•mol-1. Q1、Q2、Q3均为正值.下列说法正确的是( )
△H=-Q2kJ•mol-1. Q1、Q2、Q3均为正值.下列说法正确的是( )
| A. | 1 mol R(g)的能量总和大于1 mol M(s)与1 mol N(g) 的能量总和 | |
| B. | 将2 mol R (g)与1 mol N(g)在该条件下充分反应,放出热量Q2 kJ | |
| C. | 当1 mol M(s) 与N(g)完全转化为T (g)时(假定无热量损失),放出热量Q1+$\frac{{Q}_{2}}{2}$kJ | |
| D. | M(g)+N(g)?R(g)△H=-Q3 kJ•mol-1,则Q3<Q1 |
11.下列是三个不同短周期部分元素的原子半径及主要化合价:
试回答下列问题:
(1)五种元素中原子半径最大的元素是Na(填元素符号),画出该元素的原子结构示意图: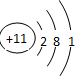
(2)W、X和Y可组成一化合物,其原子个数比为4:3:2,则该化合物属离子化合物(填“离子化合物”或“共价化合物”),存在的化学键是离子键、共价键.写出该化合物与由W、R和X按原子个数比为1:1:1组成化合物反应的化学方程式:NH4NO3+NaOH═NaNO3+NH3•H2O
(3)写出下列反应的化学方程式:Z的单质与Y元素的最高价氧化物对应的水化物反应:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
| 元素代号 | W | R | X | Y | Z |
| 原子半径/nm | 0.037 | 0.154 | 0.066 | 0.070 | 0.077 |
| 主要化合价 | +1 | +1 | -2 | -3、+5 | +2、+4 |
(1)五种元素中原子半径最大的元素是Na(填元素符号),画出该元素的原子结构示意图:
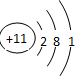
(2)W、X和Y可组成一化合物,其原子个数比为4:3:2,则该化合物属离子化合物(填“离子化合物”或“共价化合物”),存在的化学键是离子键、共价键.写出该化合物与由W、R和X按原子个数比为1:1:1组成化合物反应的化学方程式:NH4NO3+NaOH═NaNO3+NH3•H2O
(3)写出下列反应的化学方程式:Z的单质与Y元素的最高价氧化物对应的水化物反应:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
9.工业上从废铅蓄电池的铅膏回收铅的过程中,可用碳酸盐溶液与处理后的铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO32-(aq)═PbCO3(s)+SO42-(aq).某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分.
(1)上述反应的平衡常数表达式:K=$\frac{c(S{O}_{4}^{2-})}{c(C{O}_{3}^{2-})}$
(2)室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化.在Na2CO3溶液中PbSO4转化率较大,理由是相同浓度的Na2CO3和NaHCO3溶液中,前者c(CO32-)较大
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3•Pb(OH)2],它和PbCO3受热都易分解生成PbO.该课题组对固体产物(不考虑PbSO4)的成分提出如下假设.请你完成假设二和假设三:
假设一:全部为PbCO3;
假设二:全部为2PbCO3•Pb(OH)2;
假设三:PbCO3与2PbCO3•Pb(OH)2的混合物.
(4)为验证假设一是否成立,课题组进行如下研究:
①定性研究:请你完成表中内容
②定量研究:取26.7mg的干燥样品,加热,测得固体质量随温度的变化关系如下图.某同学由图中信息得出结论:假设一不成立.你是否同意该同学的结论,并简述理由:同意,若全部为PbCO3,26.7g完全分解后,其固体质量为22.3g.
0 169825 169833 169839 169843 169849 169851 169855 169861 169863 169869 169875 169879 169881 169885 169891 169893 169899 169903 169905 169909 169911 169915 169917 169919 169920 169921 169923 169924 169925 169927 169929 169933 169935 169939 169941 169945 169951 169953 169959 169963 169965 169969 169975 169981 169983 169989 169993 169995 170001 170005 170011 170019 203614
(1)上述反应的平衡常数表达式:K=$\frac{c(S{O}_{4}^{2-})}{c(C{O}_{3}^{2-})}$
(2)室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化.在Na2CO3溶液中PbSO4转化率较大,理由是相同浓度的Na2CO3和NaHCO3溶液中,前者c(CO32-)较大
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3•Pb(OH)2],它和PbCO3受热都易分解生成PbO.该课题组对固体产物(不考虑PbSO4)的成分提出如下假设.请你完成假设二和假设三:
假设一:全部为PbCO3;
假设二:全部为2PbCO3•Pb(OH)2;
假设三:PbCO3与2PbCO3•Pb(OH)2的混合物.
(4)为验证假设一是否成立,课题组进行如下研究:
①定性研究:请你完成表中内容
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取一定量样品充分干燥,然后将样品加热分解,将产生的气体依次通过盛有无水硫酸铜的干燥管和盛有澄清石灰水的烧瓶 | 若无水硫酸铜不变蓝色,澄清石灰水变浑浊,说明样品全部是PbCO3 |
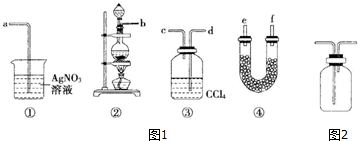
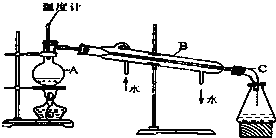 如图是某学生绘制的实验室蒸馏石油的装置图:
如图是某学生绘制的实验室蒸馏石油的装置图:
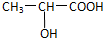
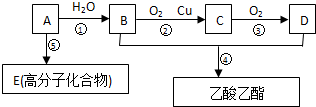
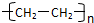

 .
.