题目内容
14.为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生少量气体.
实验二:取上述实验一后锥形瓶中清液,进行如下实验:
①该清液滴在有色布条上有极强的漂白作用.
②该清液中滴加碳酸钠溶液产生白色沉淀.
③该清液中滴加盐酸可产生大量气体.
④该清液加热后变浑浊并产生大量气体.
回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有HClO(写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有Ca2+离子;清液中滴加盐酸产生的气体是CO2;清液加热后产生浑浊的原因是因为生成了CaCO3.
(2)该学生通过上述实验,写出氯水和碳酸钙反应的化学方程式为:2CaCO3+2Cl2+H2O=CaCl2+Ca(HCO3)2+2HClO.
分析 (1)氯水中含有具有漂白作用的次氯酸;加入碳酸钠生成白色沉淀说明沉淀是碳酸钙;氯气与水反应Cl2+H2O=HCl+HClO,加入碳酸钙,观察到氯水的黄绿色褪去,同时产生少量气体,因此碳酸钙和二氧化碳和水反应生成了可溶于水的碳酸氢钙CaCO3+H2O+CO2=Ca(HCO3)2,滴加盐酸可产生大量气体,该气体是二氧化碳;加入碳酸钙,观察到氯水的黄绿色褪去,同时产生少量气体,因此碳酸钙和二氧化碳和水反应生成了可溶于水的碳酸氢钙CaCO3+H2O+CO2=Ca(HCO3)2,该清液加热后变浑浊并产生大量气体是碳酸氢钙分解生成碳酸钙沉淀和二氧化碳气体;
(2)依据反应产物中有HClO、Ca(HCO3)2、CaCl2,书写化学方程式.
解答 解:(1)清液滴在有色布条上有极强的漂白作用.说明该清液中含有具有漂白性的次氯酸;清液中滴加碳酸钠溶液产生白色沉淀.说明该清液中含有钙离子,生成沉淀碳酸钙;加热后产生浑浊的原因是因为溶液中的碳酸氢钙分解生成碳酸钙水和二氧化碳气体,生成了沉淀碳酸钙,反应方程式为Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO2↑H2O,
故答案为:HClO;Ca2+;CO2;CaCO3;
(2)根据实验二(1)-(4)实验步骤发生的反应和物质判断可知氯水和碳酸钙反应的化学方程式为2CaCO3+2Cl2+2H2O=CaCl2+Ca(HCO3)2+2HClO,
故答案为:2CaCO3+2Cl2+H2O=CaCl2+Ca(HCO3)2+2HClO.
点评 本题主要考查氯及其化合物的相关的实验,题目难度不大,答题时注意根据发生的反应正确描述反应现象.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.初步提纯下列物质(括号内为少量杂质),选用的试剂和分离方法均正确的是( )
| 序号 | 物质 | 试剂 | 分离方法 |
| ① | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| ② | 溴苯(溴) | NaOH溶液 | 分液 |
| ③ | 乙醇(水) | 生石灰 | 蒸馏 |
| ④ | 苯(环己烷) | 水 | 分液 |
| A. | ①② | B. | ①③ | C. | ②③ | D. | ④③ |
5.将煤粉隔绝空气加强热,除主要得到焦炭外,还能得到下表所列的物质:
(1)表中所列物质不属于有机物的是(填序号):②⑦,苯酚的俗称为石炭酸.
(2)能与溴水反应使之褪色的烃是(填序号):③.
(3)能发生加聚反应、生成物可用作制造食品包装袋的是(填序号)③,该物质发生加聚反应的化学方程式为nCH2=CH2$\stackrel{催化剂}{→}$
(4)能使酸性高锰酸钾褪色的烃是(填结构简)CH2=CH2、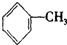 、
、 .
.
(4)彼此互为同系物的是(填序号):④⑤.
(5)甲苯的一氯取代产物的有4种,请写出甲苯的一氯取代产物结构简式: .
.
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 名称 | 甲烷 | 一氧化碳 | 乙烯 | 苯 | 甲苯 | 苯酚 | 氨水 |
(2)能与溴水反应使之褪色的烃是(填序号):③.
(3)能发生加聚反应、生成物可用作制造食品包装袋的是(填序号)③,该物质发生加聚反应的化学方程式为nCH2=CH2$\stackrel{催化剂}{→}$

(4)能使酸性高锰酸钾褪色的烃是(填结构简)CH2=CH2、
 、
、 .
.(4)彼此互为同系物的是(填序号):④⑤.
(5)甲苯的一氯取代产物的有4种,请写出甲苯的一氯取代产物结构简式:
 .
.
9.工业上从废铅蓄电池的铅膏回收铅的过程中,可用碳酸盐溶液与处理后的铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO32-(aq)═PbCO3(s)+SO42-(aq).某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分.
(1)上述反应的平衡常数表达式:K=$\frac{c(S{O}_{4}^{2-})}{c(C{O}_{3}^{2-})}$
(2)室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化.在Na2CO3溶液中PbSO4转化率较大,理由是相同浓度的Na2CO3和NaHCO3溶液中,前者c(CO32-)较大
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3•Pb(OH)2],它和PbCO3受热都易分解生成PbO.该课题组对固体产物(不考虑PbSO4)的成分提出如下假设.请你完成假设二和假设三:
假设一:全部为PbCO3;
假设二:全部为2PbCO3•Pb(OH)2;
假设三:PbCO3与2PbCO3•Pb(OH)2的混合物.
(4)为验证假设一是否成立,课题组进行如下研究:
①定性研究:请你完成表中内容
②定量研究:取26.7mg的干燥样品,加热,测得固体质量随温度的变化关系如下图.某同学由图中信息得出结论:假设一不成立.你是否同意该同学的结论,并简述理由:同意,若全部为PbCO3,26.7g完全分解后,其固体质量为22.3g.
(1)上述反应的平衡常数表达式:K=$\frac{c(S{O}_{4}^{2-})}{c(C{O}_{3}^{2-})}$
(2)室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化.在Na2CO3溶液中PbSO4转化率较大,理由是相同浓度的Na2CO3和NaHCO3溶液中,前者c(CO32-)较大
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3•Pb(OH)2],它和PbCO3受热都易分解生成PbO.该课题组对固体产物(不考虑PbSO4)的成分提出如下假设.请你完成假设二和假设三:
假设一:全部为PbCO3;
假设二:全部为2PbCO3•Pb(OH)2;
假设三:PbCO3与2PbCO3•Pb(OH)2的混合物.
(4)为验证假设一是否成立,课题组进行如下研究:
①定性研究:请你完成表中内容
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取一定量样品充分干燥,然后将样品加热分解,将产生的气体依次通过盛有无水硫酸铜的干燥管和盛有澄清石灰水的烧瓶 | 若无水硫酸铜不变蓝色,澄清石灰水变浑浊,说明样品全部是PbCO3 |
19.下列化合物中,含有非极性共价键的离子化合物是( )
| A. | Na2O | B. | N2H4 | C. | Na2S2 | D. | NH4NO3 |
6.在下列各溶液中,离子一定能大量共存的是( )
| A. | 强碱性溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ | |
| C. | 所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+ | |
| D. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
3. 反应3H2(g)+CO2(g)?CH3OH(g)+H20(g)△H<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH3OH物质的量分数的变化情况如图所示,
反应3H2(g)+CO2(g)?CH3OH(g)+H20(g)△H<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH3OH物质的量分数的变化情况如图所示,
下列判断正确的是( )
 反应3H2(g)+CO2(g)?CH3OH(g)+H20(g)△H<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH3OH物质的量分数的变化情况如图所示,
反应3H2(g)+CO2(g)?CH3OH(g)+H20(g)△H<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH3OH物质的量分数的变化情况如图所示,下列判断正确的是( )
| A. | P3>P2,T3>T2 | B. | P2>P4,T4>T2 | C. | P1>P3,T1>T3 | D. | P1>P4 T2<T3 |
1.下列实验能获得成功的是( )
| A. | 苯和溴用铁作催化剂生成溴苯 | |
| B. | 向苯酚浓溶液中滴入少量浓溴水可观察到白色三溴苯酚沉淀 | |
| C. | 氯乙烷与NaOH溶液共热,在水解后的溶液中加入硝酸酸化的AgNO3溶液检验Cl- | |
| D. | 向淀粉在酸性条件下水解的产物中加银氨溶液,水浴加热,检验葡萄糖的生成 |