8.下列说法中正确的是( )
| A. | 强电解质溶液总比弱电解质的导电性强 | |
| B. | 稀硫酸溶液中不存在H2SO4分子 | |
| C. | 氯化氢是电解质,所以液态氯化氢能导电 | |
| D. | 电解质溶液中只存在离子,没有分子 |
5.标准状况下H2S和O2混合气体100mL,经点燃后反应至完全,所得气体经干燥后,恢复到原来状况时体积为10mL,该10mL气体可能是( )
| A. | H2S | B. | O2 | C. | H2S、SO2 | D. | SO3 |
4. 对于已达到平衡的可逆反应:N2(g)+3H2(g)?NH3(g)+Q,Q>0,为使正逆反应速率符合如图所示,应采取的措施是( )
对于已达到平衡的可逆反应:N2(g)+3H2(g)?NH3(g)+Q,Q>0,为使正逆反应速率符合如图所示,应采取的措施是( )
 对于已达到平衡的可逆反应:N2(g)+3H2(g)?NH3(g)+Q,Q>0,为使正逆反应速率符合如图所示,应采取的措施是( )
对于已达到平衡的可逆反应:N2(g)+3H2(g)?NH3(g)+Q,Q>0,为使正逆反应速率符合如图所示,应采取的措施是( )| A. | 增大N2的浓度 | B. | 升高温度 | C. | 增大压强 | D. | 增大NH3的浓度 |
3.工业上用软锰矿和闪锌矿联合生产MnO2和Zn的化学方程式为:
①MnO2+ZnS+2H2SO4$\frac{\underline{\;电解\;}}{\;}$MnSO4+ZnSO4+S+2H2O
②MnSO4+ZnSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$MnO2+Zn+2H2SO4.
下列说法中错误的是( )
①MnO2+ZnS+2H2SO4$\frac{\underline{\;电解\;}}{\;}$MnSO4+ZnSO4+S+2H2O
②MnSO4+ZnSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$MnO2+Zn+2H2SO4.
下列说法中错误的是( )
| A. | 反应①中MnO2和H2SO4都是氧化剂 | |
| B. | 反应①中每析出12.8g S沉淀,转移0.8mol电子 | |
| C. | 金属锌也可用热还原法制备 | |
| D. | 硫酸在生产种可循环使用 |
2.FeCl3和CuCl2的混合溶液中加入a g铁粉,待溶液完全变为浅绿色时,滤出不溶物,经干燥后得其质量也是a g,则原溶液中FeCl3和CuCl2的物质的量比是( )
| A. | 1:7 | B. | 2:1 | C. | 2:7 | D. | 7:2 |
1.下列实验操作正确的是( )
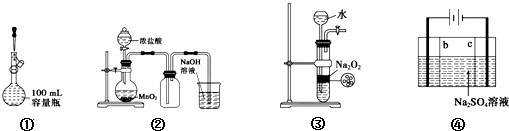

| A. | 装置①定容 | |
| B. | 装置②实验室制氯气 | |
| C. | 装置③用于制备少量氧气 | |
| D. | 利用装置④制硫酸和氢氧化钠,其中b为阴离子交换膜、c为阳离子交换膜 |
20.下列反应的离子方程式正确的是( )
0 168688 168696 168702 168706 168712 168714 168718 168724 168726 168732 168738 168742 168744 168748 168754 168756 168762 168766 168768 168772 168774 168778 168780 168782 168783 168784 168786 168787 168788 168790 168792 168796 168798 168802 168804 168808 168814 168816 168822 168826 168828 168832 168838 168844 168846 168852 168856 168858 168864 168868 168874 168882 203614
| A. | AgOH溶于氨水:AgOH+2NH3•H2O=[Ag(NH3)2]++OHˉ+2H2O | |
| B. | Na2C2O4水解:C2O42-+2H2O=H2C2O4+2OH- | |
| C. | 向NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- | |
| D. | 向酸性KMnO4溶液中通入SO2:2MnO4-+5SO2+4OH-=2Mn2++5SO42-+2H2O |