题目内容
6.某有机物0.3g完全燃烧后,生成224mL CO2 (标准状况下)和0.18g H2O,已知该物质蒸气密度是相同条件下H2密度的30倍.求:(1)该有机物的分子式;
(2)请写出它可能的结构简式.
分析 有机物的蒸气密度是相同条件下H2的30倍,则其相对分子质量为30×2=60,根据原子守恒计算有机物分子中N(C)、N(H),再结合相对分子质量计算有机物分子中N(O),据此确定有机物分子式,该有机物能与金属钠反应,至少含有-COOH、-OH中的一种,结合有机物分子式书写可能的结构.
解答 解:(1)有机物的蒸气密度是相同条件下H2的30倍,则其相对分子质量为30×2=60,该有机物0.3g完全燃烧后,生成224mL CO2 (标准状况下)和0.18g H2O,0.3g有机物的物质的量=$\frac{0.3g}{60g/mol}$=0.005mol,n(CO2)=$\frac{0.224L}{22.4L/mol}$=0.01mol,0.18g H2O的物质的量为$\frac{0.18g}{18g/mol}$=0.01mol,根据原子守恒,可知有机物分子中N(C)=$\frac{0.01mol}{0.005mol}$=2、N(H)=$\frac{0.01mol×2}{0.005mol}$=4,则有机物分子中N(O)=$\frac{60-12×2-4}{16}$=2,故有机物分子式为C2H4O2,
答:该有机物分子式为C2H4O2.
(2)有机物分子式为C2H4O2,则该有机物的结构简式为CH3COOH、HCOOCH3,
答:该有机物的结构简式为CH3COOH、HCOOCH3.
点评 本题考查有机物分子式的确定、限制条件同分异构体书写,难度不大,注意掌握燃烧法利用原子守恒确定有机物的组成.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
17.化学与生活、环境保护、资源利用等密切相关.下列说法不正确的是( )
| A. | NO2或SO2都会导致酸雨的形成 | |
| B. | 垃圾是放错地方的资源,应分类回收利用 | |
| C. | 纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 | |
| D. | 葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒 |
14.分子式为C5H10O2,能与NaOH反应且有3个甲基的同分异构体共有(不考虑立体异构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
1.下列实验操作正确的是( )
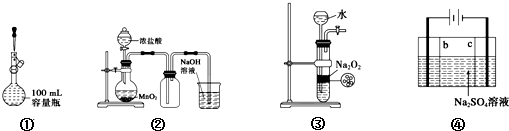

| A. | 装置①定容 | |
| B. | 装置②实验室制氯气 | |
| C. | 装置③用于制备少量氧气 | |
| D. | 利用装置④制硫酸和氢氧化钠,其中b为阴离子交换膜、c为阳离子交换膜 |
18.已知0.1mol•L-1的二元酸H2A溶液的pH=4.0,则下列说法中正确的是( )
| A. | 在Na2A、NaHA两溶液中,离子种类相同 | |
| B. | 在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等 | |
| C. | NaHA溶液pH一定大于7 | |
| D. | 在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-) |
20.以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如图所示,其中P端通入CO2.通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色.则下列说法中正确的是( )

| A. | X、Y两端都必须用铁作电极 | |
| B. | 不可以用NaOH溶液作为电解液 | |
| C. | 阴极发生的反应是:2H2O+2e-=H2↑+2OH- | |
| D. | X端为电解池的阳极 |