题目内容
2.FeCl3和CuCl2的混合溶液中加入a g铁粉,待溶液完全变为浅绿色时,滤出不溶物,经干燥后得其质量也是a g,则原溶液中FeCl3和CuCl2的物质的量比是( )| A. | 1:7 | B. | 2:1 | C. | 2:7 | D. | 7:2 |
分析 在氯化铁和氯化铜的混合溶液中加入过量的铁粉,分别发生:2Fe3++Fe=3Fe2+,Fe+Cu2+=Fe2++Cu,搅拌使其充分反应,所得固体残渣的质量与原铁粉的质量恰好相等,则消耗的铁的质量应等于生成的铜的质量,以此解答.
解答 解:设混合物中含有xmolFeCl3,ymol氯CuCl2,在FeCl3和氯CuCl2的混合溶液中加入过量的铁粉,分别发生:2Fe3++Fe=3Fe2+,Fe+Cu2+=Fe2++Cu,
搅拌使其充分反应,所得固体残渣的质量与原铁粉的质量恰好相等,则消耗的铁的质量应等于生成的铜的质量,
则(0.5x+y)×56=64y,
x:y=8:28=2:7,
故选C.
点评 本题考查混合物的计算,注意把握铁与氯化铁和氯化铜反应的方程式的书写,根据质量关系结合方程式计算,题目难度不大.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
10.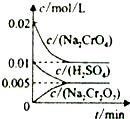 在室温下,向0.02mol/L的Na2CrO4溶液中滴加0.01mol/L的稀硫酸,溶液由黄色转变成橙红色的Na2Cr2O7,溶液中水Kw增大,在此转化过程中,各物质的量浓度变化如图所示.下列说法正确的是( )
在室温下,向0.02mol/L的Na2CrO4溶液中滴加0.01mol/L的稀硫酸,溶液由黄色转变成橙红色的Na2Cr2O7,溶液中水Kw增大,在此转化过程中,各物质的量浓度变化如图所示.下列说法正确的是( )
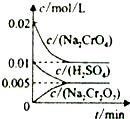 在室温下,向0.02mol/L的Na2CrO4溶液中滴加0.01mol/L的稀硫酸,溶液由黄色转变成橙红色的Na2Cr2O7,溶液中水Kw增大,在此转化过程中,各物质的量浓度变化如图所示.下列说法正确的是( )
在室温下,向0.02mol/L的Na2CrO4溶液中滴加0.01mol/L的稀硫酸,溶液由黄色转变成橙红色的Na2Cr2O7,溶液中水Kw增大,在此转化过程中,各物质的量浓度变化如图所示.下列说法正确的是( )| A. | 向以上反应加入一定量的Na2CO3溶液,对平衡几乎没有影响 | |
| B. | 升高温度,混合溶液的颜色逐渐加深 | |
| C. | 该反应的离子方程式为:2CrO42-+2H+═Cr2O72-+H2O | |
| D. | 该反应的化学平衡常数为5.0x102 |
14.如图是一套实验室制取气体的装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是( )
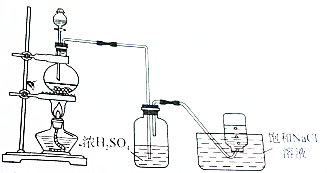

| A. | 浓H2SO4和NaCl晶体 | B. | 甲酸和浓H2SO4(制CO) | ||
| C. | MnO2和浓硫酸 | D. | 浓H3PO4和NaBr晶体 |
11.NaCl溶液中可能混有杂质NaOH、NaHCO3、Na2CO3中的一种或二种,为测定溶液中混有的杂质成分,可进行如下实验操作:分别取二份等体积混合液,用盐酸的标准液(0.10mol/L)滴定,以酚酞或甲基橙为指示剂,达到终点时消耗盐酸的体积分别为V1和V2,且V2>V1,则NaCl溶液中混有的杂质不可能为( )
| A. | NaOH | B. | Na2CO3 | C. | Na2CO3、NaHCO3 | D. | NaOH、Na2CO3 |
16.图中I是氢氧燃料电池的示意图,某同学想在II中实现Fe上镀铜,下列说法正确的是( )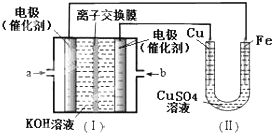

| A. | a处通入O2 | B. | b处发生氧化反应 | ||
| C. | 电流由Cu电极移向b | D. | Fe电极发生的反应为:Cu2++2e-=Cu |
 .
.