19.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,基态Y原子最外层的P能级上有1对成对电子,Z原子比X的核外电子数多4.下列说法正确的是( )
| A. | X、Y、Z的电负性大小顺序是Z<Y<X | |
| B. | Y2Z2中各原子最外层满足8e-结构,则该分子的立体构型为直线形 | |
| C. | W、X、Y、Z的原子半径最大的是X | |
| D. | W、Z形成的分子的空间构型是三角锥形 |
18.下列关于甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )
| A. |  装置:可在瓶中先装入某种液体收集NO气体 | |
| B. |  装置:可用图示的方法能检査此装置的气密性 | |
| C. |  装置:用来证明氯的非金属性比硅强 | |
| D. |  装置:橡皮管的作用是能使水顺利流下 |
17.对于可逆反应A(g)+2B(s)=2C(g)+3D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是( )
| A. | v(A)=l.5mol/(L•min) | B. | v(B)=1.2mol/(L•s) | C. | v(D)=0.4mol/(L•min) | D. | v(C)=0.2mol/(L•s) |
16.下列热化学方程式或描述中,正确的是( )
| A. | 甲烷的燃烧热为890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: N2(g)+3H2(g)═2NH3(g)△H=-38.6kJ/mol | |
| C. | 由石墨转化成金刚石需要吸收热量,则石墨比金刚石稳定 | |
| D. | lmol H2完全燃烧放热142.9kJ,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=+285.8kJ/mol |
15.下列说法正确的是( )
| A. | HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 | |
| B. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| C. | 离子键实质是阴、阳离子间的静电吸引力 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
13.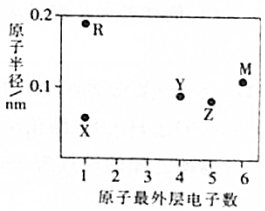 五种短周期主族元素X、Y、Z、M、R的原子半径和最外层电子数之间的关系如图所示,其中R的原子半径是短周期主族元素原子中最大的.下列说法正确的是( )
五种短周期主族元素X、Y、Z、M、R的原子半径和最外层电子数之间的关系如图所示,其中R的原子半径是短周期主族元素原子中最大的.下列说法正确的是( )
 五种短周期主族元素X、Y、Z、M、R的原子半径和最外层电子数之间的关系如图所示,其中R的原子半径是短周期主族元素原子中最大的.下列说法正确的是( )
五种短周期主族元素X、Y、Z、M、R的原子半径和最外层电子数之间的关系如图所示,其中R的原子半径是短周期主族元素原子中最大的.下列说法正确的是( )| A. | 元素的非金属性:X>Z>Y | |
| B. | M的单质常温常压下为气态 | |
| C. | X和M形成的二元化合物的水溶液呈弱酸性 | |
| D. | Y、Z、M的最高价氧化物的水化物均为强酸 |
12.从海水中提取溴的流程如图所示.下列有关说法错误的是( )


| A. | X试剂可以是SO2 | |
| B. | 步骤Ⅲ反应的离子方程式为2Br-+Cl2=2C1-+Br2 | |
| C. | 步骤IV包含萃取、分液和蒸馏 | |
| D. | 当生成1mol Br2时.需要消耗22.4L C12 |
11.已知反应X+Y=W+N为放热反应.下列说法正确的是( )
| A. | 断裂X和Y中的化学键所吸收的能量一定高于形成M和N中的化学键所放出的能量 | |
| B. | 该反应不必加热就一定可以发生 | |
| C. | 参加反应的Y的能量一定于生成的N的能量 | |
| D. | 参加反应的X和Y的总能量-定高于生成的M和N的总能量 |
10.下列指定反应的离子方程式正确的是( )
0 163699 163707 163713 163717 163723 163725 163729 163735 163737 163743 163749 163753 163755 163759 163765 163767 163773 163777 163779 163783 163785 163789 163791 163793 163794 163795 163797 163798 163799 163801 163803 163807 163809 163813 163815 163819 163825 163827 163833 163837 163839 163843 163849 163855 163857 163863 163867 163869 163875 163879 163885 163893 203614
| A. | 稀硫酸与氢氧化钡溶液混合:Ba2++OH-+H++SO42-═BsSO4↓+H2O | |
| B. | 小苏打与稀盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 工业上电解熔融状态的氯化镁:MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑ | |
| D. | 向碳酸氢铵溶液中加入足量澄清石灰水:NH4++HCO3-+Ca2++2OH-═CaCO3↓+NH3•H2O+H2O |
