题目内容
13.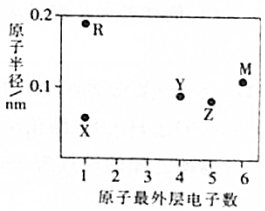 五种短周期主族元素X、Y、Z、M、R的原子半径和最外层电子数之间的关系如图所示,其中R的原子半径是短周期主族元素原子中最大的.下列说法正确的是( )
五种短周期主族元素X、Y、Z、M、R的原子半径和最外层电子数之间的关系如图所示,其中R的原子半径是短周期主族元素原子中最大的.下列说法正确的是( )| A. | 元素的非金属性:X>Z>Y | |
| B. | M的单质常温常压下为气态 | |
| C. | X和M形成的二元化合物的水溶液呈弱酸性 | |
| D. | Y、Z、M的最高价氧化物的水化物均为强酸 |
分析 R的原子半径是短周期主族元素原子中最大的,则R为Na,X的最外层电子数为1,且X的原子半径最小,则X为H;结合图中原子半径和最外层电子数之间的关系可知,Y、Z位于第二周期,M位于第三周期,Y的最外层电子数为4,则Y为C,Z的最外层电子数为5,Z为N;M的最外层电子数为6,则M为S,以此来解答.
解答 解:由上述分析可知,X为H,R为Na,Y为C,Z为N,M为S,
A.甲烷、氨气中H为正价,硝酸的酸性大于碳酸的酸性,则非金属性为Z>Y>X,故A错误;
B.M的单质常温常压下为固体,故B错误;
C.X和M形成的二元化合物为H2S,为二元弱酸,水溶液呈弱酸性,故C正确;
D.Y、Z、M的最高价氧化物的水化物中,碳酸为弱酸,硝酸、硫酸为强酸,故D错误;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子半径、最外层电子数、元素周期律来推断元素为解答的关键,侧重分析与应用能力的考查,注意R为Na是元素推断的突破口,题目难度不大.

练习册系列答案
相关题目
3.下列关于单糖和多糖相比较的叙述中,错误的是( )
| A. | 单糖可溶于水,多糖一般不溶于水 | B. | 单糖和多糖的分子中都含有羟基 | ||
| C. | 多糖可水解,单糖不能水解 | D. | 多糖和单糖均属于高分子化合物 |
1.在下列叙述的实验中能获得成功的是( )
| A. | 苯和溴水反应制取溴苯 | |
| B. | 用碘水可以检验淀粉是否已经水解 | |
| C. | 用浓溴水可以除去苯中含有的苯酚 | |
| D. | 用银氨溶液可以检验某有机物分子中是否含有醛基 |
18.下列关于甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )
| A. |  装置:可在瓶中先装入某种液体收集NO气体 | |
| B. |  装置:可用图示的方法能检査此装置的气密性 | |
| C. |  装置:用来证明氯的非金属性比硅强 | |
| D. |  装置:橡皮管的作用是能使水顺利流下 |
2.下列离子组一定能大量共存的是( )
| A. | pH=12的溶液:K+、Na+、CH3COO-、Br- | |
| B. | 由水电离出c(H+)=10-3mol/L的溶液中:Na+、[Al(OH)4]-、NO3-、HCO3- | |
| C. | 无色溶液中可能大量共存在Fe3+、NH4+、Cl-、S2- | |
| D. | 1mol/L的KNO3溶液:H+、Fe2+、Cl-、SO42- |

 .
.
 .
.