10.下列说法错误的是( )
| A. | O2与O3互为同素异形体 | B. |  和 和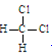 互为同分异构体 互为同分异构体 | ||
| C. | 35Cl和37Cl 互为同位素 | D. |  互为同分异构体 互为同分异构体 |
9.设NA为阿伏伽德罗常数的值,下列叙述正确的为( )
| A. | 密闭容器中2molNO 和 1molO2 充分反应,产物的分子数为2NA | |
| B. | 常温下,1L0.1mol/LnaCO3 溶液中含有的离子总数为0.3 NA | |
| C. | 0.1mol铁在0.1molCl2 中充分燃烧,转移的电子数为0.3 NA | |
| D. | 标况下,1.12L16O2 和1.12L18O2 均含有 0.1 NA个氧原子 |
7.对于反应IBr+H2O=HBr+HIO的说法正确的是( )
| A. | IBr只作氧化剂 | B. | IBr只作还原剂 | ||
| C. | IBr既不是氧化剂,又不是还原剂 | D. | IBr既是氧化剂,又是还原剂 |
5.下列说法中,正确的一组是( )
①两种元素构成的共价化合物分子中的化学键都是极性键
②两种非金属元素原子间形成的化学键都是极性键
③含有极性键的化合物分子一定不含非极性键
④只要是离子化合物,其熔点就比共价化合物的熔点高
⑤离子化合物中含有离子键
⑥分子晶体中的分子不含有离子键
⑦分子晶体中的分子内一定有共价键
⑧原子晶体中一定有非极性共价键.
①两种元素构成的共价化合物分子中的化学键都是极性键
②两种非金属元素原子间形成的化学键都是极性键
③含有极性键的化合物分子一定不含非极性键
④只要是离子化合物,其熔点就比共价化合物的熔点高
⑤离子化合物中含有离子键
⑥分子晶体中的分子不含有离子键
⑦分子晶体中的分子内一定有共价键
⑧原子晶体中一定有非极性共价键.
| A. | ②⑤⑥⑦ | B. | ①②③⑤⑥ | C. | ②⑤⑥ | D. | ②③⑤⑥⑦ |
3.用下列实验装置完成对应的实验(部分仪器已省略》,能达到实验目的是(已知HCl、NH3是极易溶于水的气体)( )
| A. | 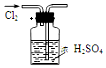 干燥Cl2 | B. |  吸收HCl | ||
| C. |  用自来水制蒸馏水 | D. |  吸收NH3 |
2.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
0 163217 163225 163231 163235 163241 163243 163247 163253 163255 163261 163267 163271 163273 163277 163283 163285 163291 163295 163297 163301 163303 163307 163309 163311 163312 163313 163315 163316 163317 163319 163321 163325 163327 163331 163333 163337 163343 163345 163351 163355 163357 163361 163367 163373 163375 163381 163385 163387 163393 163397 163403 163411 203614
| A. | SO2、SiO2、CO、P2O5都是非金属元素形成的氧化物,均为酸性氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有氧化性,都是氧化性酸 | |
| C. | BaCl2、Ca(OH)2、HNO3、HT 均为化合物 | |
| D. | HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
 ;B:
;B: ;C:
;C: .
. ;E:
;E: ;F:
;F: .
.