��Ŀ����
8��������ѧ֪ʶ�ش�����������1����ѧѧϰ���кܶ����硰A+B��C+D���ķ�Ӧ�������ʽ��A��B��C��D��Ϊ���10������������AΪ�����ӣ�BΪ�����ӣ�C��D��Ϊ���ӣ���C����Է���������D��1����
��A+B��C+D��ʾ�����ӷ���ʽΪNH4++OH- $\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��
�ڱ�״���£���2.24L��D��50mL 1mol/L�������գ���������Һ�и�����Ũ�ȴӴ�С��˳��Ϊc��NH4+����c��SO42-����c��H+����c��OH-����
��2����֪�ڳ��³�ѹ�£�
��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H=-a kJ•mol-1
��2CO��g��+O2��g��=2CO2��g����H=-b kJ•mol-1
��H2O��g��=H2O��l����H=-c kJ•mol-1
��CH3OH��l��+O2��g��=��CO��g����+2H2O��l����H=$\frac{b-a-4c}{2}$ kJ•mol-1��
��3����ѧ��ѧ�ڽ��г�����Ӧ��ʵ���У��жϳ����Ѿ���ȫ�ķ��������ϲ���Һ�У���ȡ�����ϲ���Һ����С�Թ��У��μӳ�������������ٲ���������˵�������Ѿ���ɣ�����Ҫ�ù��˵ķ��������ڻ�ѧ��Ӧ�в����ij��������ڹ�������ϴ�ӳ����IJ�������������м�������ˮ��ֱ��ˮ����ȫ��û�������ˮ��Ȼ������ظ�����2��3�Σ�
��4�������������������������ھ�ˮ����ԭ����Fe3++3H2O�TFe��OH��3�����壩+3H+�������ӷ���ʽ��ʾ������ʹ��ʱ����������������ʹ���Է�ˮ�е������������ȥ����ԭ�������Խ�ǿ��Һ��H+����Fe3+ˮ�⣬�ò���Fe��OH��3���壬�ʲ��ܾ�ˮ��
���� ��1��A��B��C��D��Ϊ���10������������AΪ�����ӣ�BΪ�����ӣ�C��D��Ϊ���ӣ���C����Է���������D��1��ӦΪNH4+��OH-�ķ�Ӧ������NH3��H2O��
��2����2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H=-a kJ•mol-1
��2CO��g��+O2��g��=2CO2��g����H=-b kJ•mol-1
��H2O��g��=H2O��l����H=-c kJ•mol-1
��ϸ�˹���ɼ��㣬����-��+4���ۣ���$\frac{1}{2}$�õ�CH3OH��l��+O2��g��=CO��g��+2H2O��l����Ӧ���ʱ䣻
��3������Һ���Լ�����������Ӧ��������Ѿ���ȫ���ڹ�������ϴ�ӳ�����ʹ����ˮ��û������ˮ��Ȼ���£��Դ������
��4��������ˮ�����ɽ��壬���������ԣ�������Һ���������ӵ�ˮ�⣮
��� �⣺��1��A��B��C��D��Ϊ���10������������AΪ�����ӣ�BΪ�����ӣ�C��D��Ϊ���ӣ���C����Է���������D��1��ӦΪNH4+��OH-�ķ�Ӧ������NH3��H2O��
��A+B��C+D��ʾ�����ӷ���ʽΪNH4+��OH-�ķ�Ӧ������ʽΪNH4++OH- $\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��
�ʴ�Ϊ��NH4++OH- $\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��
��DΪNH3����2.24L��D��50mL 1mol/L�������գ���Ӧ���ɣ�NH4��2SO4��Ϊǿ�������Σ�ˮ������ԣ�����Ũ�ȴ�С˳��Ϊc��NH4+����c��SO42-����c��H+����c��OH-����
�ʴ�Ϊ��c��NH4+����c��SO42-����c��H+����c��OH-����
��2����2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H=-a kJ•mol-1
��2CO��g��+O2��g��=2CO2��g����H=-b kJ•mol-1
��H2O��g��=H2O��l����H=-c kJ•mol-1
��ϸ�˹���ɼ��㣬����-��+4���ۣ���$\frac{1}{2}$�õ�CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=$\frac{b-a-4c}{2}$KJ/mol��
�ʴ�Ϊ��$\frac{b-a-4c}{2}$��
��3���ڽ��г�����Ӧ��ʵ��ʱ�����ϲ�����Һ�μ���Һ���μ��Լ����������ɳ��������϶������Ѿ���ȫ���ڹ�������ϴ�ӳ����IJ��������Ų������������ע������ˮ��û������ˮ��Ȼ���£��ظ�2��3�Σ�
�ʴ�Ϊ�����ϲ���Һ�У���ȡ�����ϲ���Һ����С�Թ��У��μӳ�������������ٲ���������˵�������Ѿ���ɣ���������м�������ˮ��ֱ��ˮ����ȫ��û�������ˮ��Ȼ������ظ�����2��3�Σ�
��4�������������������������ھ�ˮ����ԭ����Fe3++3H2O?Fe��OH��3+3H+�����ɽ��壬���������ԣ��ɾ���ˮ�����������������������ӵ�ˮ�⣬�����������������壬����ʹ�����������ȥ��
�ʴ�Ϊ��Fe3++3H2O�TFe��OH��3�����壩+3H+�����Խ�ǿ��Һ��H+����Fe3+ˮ�⣬�ò���Fe��OH��3���壬�ʲ��ܾ�ˮ��
���� ���⿼��������ƶϡ�ʵ����������������ڿ������ӷ�Ӧ����ʽ����д����Ϥ�����ķ�Ӧ���ɽ��ע����Ŀ�е���Ϣ����ѧ֪ʶ�Ľ�����ж����ʼ�Ũ�ȵļ�����������Ŀ�Ѷ��еȣ�

 ���ݼ���ϵ�д�
���ݼ���ϵ�д�| A�� | 1mol���ᣨ ������1mol Na��ȫ��Ӧ ������1mol Na��ȫ��Ӧ | |
| B�� | һ�ȼ��飨CH3Cl���Ͷ������飨ClCH2CH2Cl����ͬϵ�� | |
| C�� | ������2��ͬ���칹�壬��˶���Ҳ������ͬ���칹�� | |
| D�� | ��ϩ��ʹ��ˮ��ɫ����ϩ�����������7��ԭ��λ��ͬһƽ���� |
| A�� | 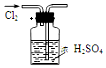 ����Cl2 | B�� |  ����HCl | ||
| C�� |  ������ˮ������ˮ | D�� |  ����NH3 |
| A�� | C+O2 $\frac{\underline{\;\;��\;\;}}{\;}$CO2 | B�� | HCl+NaOH=NaCl+H2O | ||
| C�� | 2KClO3$\frac{\underline{\;\;��\;\;}}{\;}$2KCl+3O2�� | D�� | Zn+2HCl=ZnCl2+H2�� |
| A�� | ���ǵķ�����Ŀ֮��Ϊ1��1 | B�� | ����������ԭ����Ŀ֮��Ϊ2��3 | ||
| C�� | ��������ԭ����Ŀ֮��Ϊ3��4 | D�� | ���ǵ�����֮��Ϊ1��1 |
| A�� | ��ͭ��⾫��ʱ���������Һ����ɺ�Ũ�Ⱦ����ֲ��� | |
| B�� | ����Ʒ�϶�һ����ȵ�п�㣬ѡ��п���������Ƽ�����������п���ӵ���Һ�����Һ | |
| C�� | ����Ȼ�����Һ�����Ʊ������� | |
| D�� | �ȼҵ�У���ⱥ��ʳ��ˮʱ�������ϲ���Cl2��NaOH |
| A�� | ������ˮ | B�� | Ư�۵�ˮ��Һ | C�� | ����������Һ | D�� | �������� |
 ����0.5mol HCl��0.5mol MgSO4�Ļ����Һ������1mol•L-1��Ba��OH��2��Һ����ͨ�����㲢��������Ϊ�������ʵ�����������Ϊ����Ba��OH��2��Һ�������ͼ��
����0.5mol HCl��0.5mol MgSO4�Ļ����Һ������1mol•L-1��Ba��OH��2��Һ����ͨ�����㲢��������Ϊ�������ʵ�����������Ϊ����Ba��OH��2��Һ�������ͼ��