20.下列说法错误的是(用NA代表阿伏加德罗常数的值)( )
| A. | 32g O2所含的原子数目为2NA | |
| B. | 0.5NA个氯气分子的物质的量是0.5mol | |
| C. | 在标准状况下,22.4 L CH4与18 g H2O所含有电子数均为10NA | |
| D. | 22.4 L的CO气体与1 mol N2所含的电子数相等 |
19.下列说法正确的是( )
| A. | 摩尔质量就是物质的相对分子质量 | B. | 摩尔质量就1mol物质所具有的质量 | ||
| C. | HNO3的摩尔质量是63g | D. | 硫酸和磷酸的摩尔质量相等 |
18.下列溶液中有关物质的量浓度关系正确的是( )
| A. | NaB溶液的pH=8,c(Na+)-c(B-)=0.99×10-6 mol•L-1 | |
| B. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液,c(NaOH)<c(CH3COONa)<c(Na2CO3) | |
| C. | 0.2mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合:(H+)=c(OH-)+c(HCO3-)+2c(H2CO3) | |
| D. | 0.1 mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
16.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是氯碱工业的主要原料.下列说法正确的是( )
| A. | C和E的单质常温下不能相互反应 | |
| B. | C与B形成的两种化合物均属于离子化合物,且化学键类型完全相同 | |
| C. | 原子半径:C>D>A>B | |
| D. | A、D、E的最高价氧化物对应水化物均为弱酸 |
14.已知某有机物A的核磁共振氢谱如图所示,下列说法中错误的是( )

| A. | 若A的分子式为C3H6O2,则其结构简式为CH3COOCH3 | |
| B. | 由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子,且个数之比为1:2:3 | |
| C. | 仅由其核磁共振氢谱无法得知其分子中的氢原子总数 | |
| D. | 若A的化学式为C3H6O2,则其同分异构体有三种 |
13.提出碳价四面体学说的科学家是( )
| A. | 凯库勒 | B. | 李比希 | C. | 范霍夫 | D. | 库恩 |
11.室温下,A、B两烧杯均盛有10mlpH=2的HA酸溶液,向B烧杯中加水稀释至pH=3,关于A、B两烧杯中溶液的描述正确的是( )
0 162956 162964 162970 162974 162980 162982 162986 162992 162994 163000 163006 163010 163012 163016 163022 163024 163030 163034 163036 163040 163042 163046 163048 163050 163051 163052 163054 163055 163056 163058 163060 163064 163066 163070 163072 163076 163082 163084 163090 163094 163096 163100 163106 163112 163114 163120 163124 163126 163132 163136 163142 163150 203614
| A. | 水电离出的OH-浓度:10c(OH-)A>c(OH-)B | |
| B. | 溶液的体积:10VA≤VB | |
| C. | 若分别用等浓度的氢氧化钠溶液完全中和,所得溶液的pH:A>B | |
| D. | 若分别与10mLpH=12的氢氧化钠溶液反应,所得溶液的pH:A≤B |
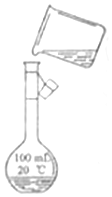 为除去粗盐中的CaCl2、MgCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的CaCl2、MgCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):