题目内容
18.下列溶液中有关物质的量浓度关系正确的是( )| A. | NaB溶液的pH=8,c(Na+)-c(B-)=0.99×10-6 mol•L-1 | |
| B. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液,c(NaOH)<c(CH3COONa)<c(Na2CO3) | |
| C. | 0.2mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合:(H+)=c(OH-)+c(HCO3-)+2c(H2CO3) | |
| D. | 0.1 mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
分析 A.NaB溶液呈碱性,说明NaB为强碱弱酸盐,溶液中存在电荷守恒,根据电荷守恒判断;
B、碳酸氢根离子的酸性弱于醋酸的酸性,所以等浓度的CH3COONa和Na2CO3,碳酸钠的碱性强;
C、0.2mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,生成等物质的量浓度的碳酸钠和碳酸氢钠,根据物料守恒和电荷守恒分析解答;
D、0.1 mol•L-1的NaHA溶液,其pH=4:说明电离程度大于水解程度;
解答 解:A.NaB溶液呈碱性,说明NaB为强碱弱酸盐,溶液中存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(B-),所以c(Na+)-c(B-)=c(OH-)-c(H+)=10-6mol/L-10-8mol/L=0.99×10-6mol/L,故A正确;
B、碳酸氢根离子的酸性弱于醋酸的酸性,所以等浓度的CH3COONa和Na2CO3,碳酸钠的碱性强,所以pH相等的CH3COONa、NaOH和Na2CO3三种溶液,c(NaOH)<c(Na2CO3)<c(CH3COONa),故B错误;
C、0.2mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,生成等物质的量浓度的碳酸钠和碳酸氢钠,根据物料守恒和电荷守恒可得:2c(OH-)+c(CO32-)=3c(H2CO3)+2(H+)+c(HCO3-),故C错误;
D、0.1 mol•L-1的NaHA溶液,其pH=4:说明电离程度大于水解程度,所以离子浓度大小为:c(HA-)>c(H+)>c(A2-)>c(H2A),故D错误;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,明确反应后溶质组成为解答关键,注意掌握盐的水解原理、电荷守恒、物料守恒及质子守恒的含义,能够根据盐的水解原理及守恒知识判断各离子浓度大小.

| A. | 凯库勒 | B. | 李比希 | C. | 范霍夫 | D. | 库恩 |
| A. | 容器内压强不再改变 | B. | 水的消耗速率等于氢气的生成速率 | ||
| C. | 气体的密度不再改变 | D. | 反应不再进行 |
| A. | 钠和水反应2Na+H2O═2Na++OH-+H2↑ | |
| B. | 氯化镁溶液加入氨水:Mg2++2OH-═Mg(OH)2↓ | |
| C. | 氯气与水反应:Cl2+H2O?H++Cl-+HClO | |
| D. | 氢氧化钡与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
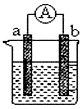 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: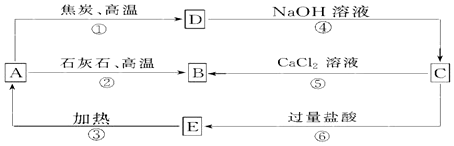
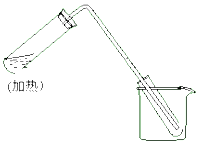 如图是用自来水制取少量蒸馏水的简易装置,(加热及固定仪器略),其原理与教材中实验完全相同.回答下列问题:
如图是用自来水制取少量蒸馏水的简易装置,(加热及固定仪器略),其原理与教材中实验完全相同.回答下列问题: