题目内容
17.已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O若19.2g铜与足量硝酸完全反应,则消耗硝酸为0.8mol,被还原的硝酸为0.2mol,生成NO的体积为4.48L(标准状况).
分析 19.2g铜的物质的量为:$\frac{19.2g}{64g/mol}$=0.3mol,由3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O反应可知3mol的铜,消耗8mol的硝酸,生成2mol的一氧化氮气体,由此分析解答.
解答 解:19.2g铜的物质的量为:$\frac{19.2g}{64g/mol}$=0.3mol,由3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O反应可知3mol的铜,消耗8mol的硝酸,被还原的硝酸为2mol,生成2mol的一氧化氮气体,所以0.3mol的铜消耗硝酸 0.8 mol,被还原的硝酸为0.2mol,生成 NO的体积为 4.48L,
故答案为:0.8;0.2;4.48.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意基本概念的应用,题目难度不大.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
5.下列表示物质结构的化学用语或模型正确的是( )
| A. | N2的电子式为 N:::N | B. | CH4分子的球棍模型: | ||
| C. | HClO的结构式为H-O-Cl | D. | 氟离子的结构示意图: |
2.下列关于容量瓶的相关叙述中正确的是( )
| A. | 容量瓶上标有:①浓度、②容量、③刻度线 | |
| B. | 使用容量瓶前应先检查它是否漏水 | |
| C. | 容量瓶先用蒸馏水洗净,再用待配液润洗 | |
| D. | 氢氧化钠溶解后可马上转移到容量瓶中 |
9.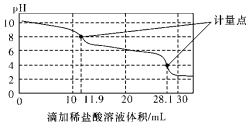 实验室使用pH传感器来测定Na2CO3和NaHCO3混合物中NaHCO3的含量.称取1.59g样品,溶于水配成250.00mL溶液,取出该溶液25.00mL用0.1mol•L-1盐酸进行滴定,得到如图曲线.以下说法或操作正确的是( )
实验室使用pH传感器来测定Na2CO3和NaHCO3混合物中NaHCO3的含量.称取1.59g样品,溶于水配成250.00mL溶液,取出该溶液25.00mL用0.1mol•L-1盐酸进行滴定,得到如图曲线.以下说法或操作正确的是( )
 实验室使用pH传感器来测定Na2CO3和NaHCO3混合物中NaHCO3的含量.称取1.59g样品,溶于水配成250.00mL溶液,取出该溶液25.00mL用0.1mol•L-1盐酸进行滴定,得到如图曲线.以下说法或操作正确的是( )
实验室使用pH传感器来测定Na2CO3和NaHCO3混合物中NaHCO3的含量.称取1.59g样品,溶于水配成250.00mL溶液,取出该溶液25.00mL用0.1mol•L-1盐酸进行滴定,得到如图曲线.以下说法或操作正确的是( )| A. | 上一个计量点前发生反应的离子方程式为HCO3-+H+═H2O+CO2↑ | |
| B. | 下一个计量点溶液中存在大量的阴离子是Cl-、HCO3- | |
| C. | 此样品n(NaHCO3)=(28.1-2×11.9)×10-4 mol | |
| D. | 使用该方法测定Na2CO3和NaOH混合溶液中的氢氧化钠含量,将会得到1个计量点 |
6.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 常温常压下,2.3 g Na变成Na2O2时,失去0.2NA个电子 | |
| B. | 常温常压下,32 g氧气和32 g臭氧都含有2NA个氧原子 | |
| C. | 含0.2 mol NaOH的溶液中含有NA个Na+离子 | |
| D. | 22.4LCO和CO2的混合气体中所含的碳原子数一定是NA |
7.下列说法正确的是( )
| A. | 离子化合物中只能含有离子键 | |
| B. | 化学反应的过程,本质上是旧化学键断裂和新化学键形成的过程 | |
| C. | 化学键存在于分子之间 | |
| D. | 共价化合物中可能含有离子键 |