13.化合物X是一种医药中间体,其结构简式如图所示.下列有关X的说法正确的是( )
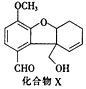

| A. | 分子中含2个手性碳原子 | |
| B. | 分子中所有碳原子均处于同一平面 | |
| C. | 能发生银镜反应,不能发生酯化反应 | |
| D. | 1molX最多能与4molH2发生加成反应 |
12.为制取含HClO浓度较高的溶液,下列图示装置和原理均正确,且能达到实验目的是( )
| A. | 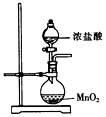 制取氯气 | B. | 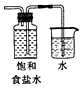 制取氯水 | C. | 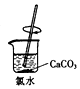 提高HClO浓度 | D. | 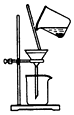 过滤 |
11.下列有关物质的性质与用途具有对应关系的是( )
| A. | 液氨气化吸热,可用作制冷剂 | B. | 明矾易溶于水,可用作净水剂 | ||
| C. | 盐酸具有还原性,可用于除去铁锈 | D. | 浓硝酸其有酸性,可用于钝化铁、铝 |
10.碳是构成地球生命的重要元素.下列说法正确的是( )
| A. | 自然界中不存在游离态的碳 | B. | 碳的化合物数量众多,分布极广 | ||
| C. | 向空气中排放二氧化碳会形成酸雨 | D. | 煤、石油、天然气属于可再生碳资源 |
8. LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )
LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )
 LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )
LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )| A. | B极区电解液为LiOH溶液 | |
| B. | 每产生标准状况下2.24L氢气,就有0.1 mol阳离子通过交换膜进入阴极区 | |
| C. | 电解过程中Li+向B电极迁移 | |
| D. | 阳极电极反应式为2Cl--2e-=Cl2↑ |
7.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,56g由N2和CO组成的混合气体含有的原子数目为4 NA | |
| B. | 高温下,0.2 molFe与足量水蒸气反应,生成的H2分子数为0.3NA | |
| C. | 1 L 1.0mol•L-1的NaAlO2水溶液中含有的总原子数为2NA | |
| D. | 1 mol羟基中含有的电子数为10NA |
6.下列由实验现象得出的结论正确的是( )
| 选项 | 实验及现象 | 结论 |
| A | 向AgNO3和AgCl的浊液中滴入0.1mol/LNa2S溶液,生成黑色沉淀 | Ag2S的溶度积比AgCl的小 |
| B | 将光亮镁条放入盛有NH4Cl溶液的试管中,产生大量气泡,同时将湿润的红色石蕊试纸靠近试管口,试纸变蓝 | 反应产生的气体一定是NH3 |
| C | 向溶液X中先滴加稀硝酸,在滴加Ba(NO3)2溶液,出现白色沉淀 | 溶液X中一定含有SO42- |
| D | 将铜粉加入1.0mol/L Fe2(SO4)3溶液中,溶液变蓝 | 说明氧化性Fe3+>Cu2+ |
| A. | A | B. | B | C. | C | D. | D |
4.有机物甲的分子式为C7H14O2,在酸性条件下甲水解为乙和丙两种有机物,且乙和丙分子中含有数目相同的甲基,在相同的温度和压强下,同质量的乙和丙的蒸气所占体积相同,则甲的可能结构有( )
0 162763 162771 162777 162781 162787 162789 162793 162799 162801 162807 162813 162817 162819 162823 162829 162831 162837 162841 162843 162847 162849 162853 162855 162857 162858 162859 162861 162862 162863 162865 162867 162871 162873 162877 162879 162883 162889 162891 162897 162901 162903 162907 162913 162919 162921 162927 162931 162933 162939 162943 162949 162957 203614
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
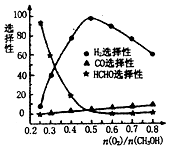 碳元素及其化合物与人类的生活、生产息息相关,请回答下列问题:
碳元素及其化合物与人类的生活、生产息息相关,请回答下列问题: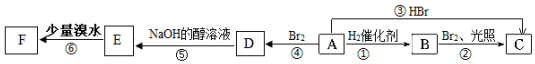
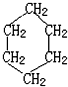 (结构简式).
(结构简式).