题目内容
13.化合物X是一种医药中间体,其结构简式如图所示.下列有关X的说法正确的是( )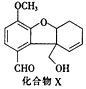
| A. | 分子中含2个手性碳原子 | |
| B. | 分子中所有碳原子均处于同一平面 | |
| C. | 能发生银镜反应,不能发生酯化反应 | |
| D. | 1molX最多能与4molH2发生加成反应 |
分析 有机物含有醛基、羟基、碳碳双键等官能团,具有醛、醇和烯烃的性质,结合有机物的结构特点解答该题.
解答 解:A.手性碳原子连接4个不同的原子或原子团,分子中五元环中连接O、-OH的碳为手性碳原子,共2个,故A正确;
B.含有饱和碳原子,具有甲烷的结构特点,则所有的碳原子不可能共平面,故B错误;
C.含有醛基,可发生银镜反应,含有羟基,可发生酯化反应,故C错误;
D.能与氢气反应的为苯环、醛基和碳碳双键,则1molX最多能与5molH2发生加成反应,故D错误.
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意常见官能团的性质,题目难度不大.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
3.下列条件变化,一定使任何反应的正、逆反应速率都增大的是( )
| A. | 缩小反应容器的体积 | B. | 增加反应物的物质的量 | ||
| C. | 升高温度 | D. | 增加催化剂的用量 |
1.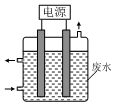 用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
 用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )| A. | 除去CN-的反应:2CN-+5ClO-+2H+═N2↑+2CO2↑+5Cl-+H2O | |
| B. | 阳极的电极反应式为:Cl-+2OH--2e-═ClO-+H2O | |
| C. | 阴极的电极反应式为:2H2O+2e-═H2↑+2OH- | |
| D. | 用石墨作阳极,铁作阴极 |
8. LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )
LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )
 LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )
LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )| A. | B极区电解液为LiOH溶液 | |
| B. | 每产生标准状况下2.24L氢气,就有0.1 mol阳离子通过交换膜进入阴极区 | |
| C. | 电解过程中Li+向B电极迁移 | |
| D. | 阳极电极反应式为2Cl--2e-=Cl2↑ |
18.按照有机物的命名规则,下列命名正确的是( )
| A. | 1,2-二甲基戊烷 | B. | 2-乙基丁烷 | C. | 3-乙基己烷 | D. | 3,4-二甲基戊烷 |
5.我国科研人员以Zn和尖晶石型锰酸锌(ZnMn2O4)为电极材料,研制出一种水系锌离子电池.该电池的总反应方程式:xZn+Zn1-xMn2O4$?_{放电}^{充电}$ZnMn2O4(0<x<1).下列说法正确的是( )
| A. | 充电时,Zn2+向ZnMn2O4电极迁移 | |
| B. | 充电时,阳极反应:ZnMn2O4-2xe-═Zn1-xMn2O4+xZn2+ | |
| C. | 放电时,每转移1mol e-,ZnMn2O4电极质量增加65g | |
| D. | 充放电过程中,只有Zn元素的化合价发生变化 |
2.下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 测定等浓度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金属:S>C |
| B | 向雨水中加入少量硫酸铁 | 容器底部出现不溶物 | 铁盐具有杀菌作用 |
| C | 向蔗糖中加入浓H2SO4 | 蔗糖变黑,并放出有刺激性气味的气体 | 浓H2SO4具有脱水性 |
| D | 有色布条放入盛满干燥的Cl2的集气瓶中,盖上玻璃片 | 布条不褪色 | 干燥的Cl2不能漂白 |
| A. | A | B. | B | C. | C | D. | D |
 A、B、C、D、E是前四周期的核电荷数依次增大元素,A原子核外s轨道电子数是p轨道电子数的2倍,C、D同一主族,D元素原子M层有一对成对的p电子,元素E位于周期表ⅠB族.请回答下列相关问题(涉及元素的请用对应的元素符号冋答)
A、B、C、D、E是前四周期的核电荷数依次增大元素,A原子核外s轨道电子数是p轨道电子数的2倍,C、D同一主族,D元素原子M层有一对成对的p电子,元素E位于周期表ⅠB族.请回答下列相关问题(涉及元素的请用对应的元素符号冋答)